A nociceptorokat háromféle ingerrel lehet aktiválni a célszöveten belül – hőmérséklet (termikus), mechanikus (pl. Nyújtás / törzs) és kémiai (pl. PH-változás) helyi gyulladásos folyamat eredményeként). Így a káros inger e három csoport egyikébe sorolható.
A nociception és a fájdalom kifejezéseket nem szabad szinonimán használni, mert mindegyik előfordulhat a másik nélkül. A nociceptorok aktiválásából fakadó fájdalmat nociceptív fájdalomnak nevezzük. A nociceptív fájdalom a szövet szerint osztályozható, amelyben a nociceptor aktiválódott: felszíni szomatikus (pl. Bőr), mély szomatikus (pl. Szalagok / inak / csontok / izmok) vagy zsigeri (belső szervek).
Nociception útja
Nem minden nociceptor reagál minden típusra ártalmas ingerekről. A káros ingerre adott válasz nyilvánvaló hiánya a végterminál (szabad idegvégződés) membránján elhelyezkedő különböző receptorok miatt következhet be, vagy az inger intenzitása nem megfelelő. Általában a nociceptor stimulációs küszöbe a szövetkárosító intenzitás alatt van. A nociceptorok heterogén tulajdonságokkal rendelkeznek, reagálva az inger többféle modalitására (polimodális). Azonban egy modalitás káros ingerének alkalmazása megváltoztathatja a nociceptor reakció tulajdonságait más modalitásokra. Ezenkívül egy adott inger adott ideig történő alkalmazása hosszú távú változásokat indukálhat a nociceptor válaszjellemzőiben. A sérülés és a megerősítés csökkenti a küszöbértéket, és növeli az adott ingerre adott válasz nagyságát, ezt a jelenséget perifériás szenzibilizációnak nevezik. Különösen érdekes a hőre érzékeny, de mechanikailag érzéketlen nemmelinizált afferensek, amelyek mechanikai érzékenységet csak a sérülés hátterében fejlesztenek ki.
A nociceptorok szabad idegvégződések morfológiai megjelenésével bírnak. A “szabad idegvégződés” kifejezés azt jelzi, hogy a fénymikroszkópban nem ismerhető fel (korpuszkuláris) receptív szerkezet. Jelenleg nincsenek egyértelmű ultrastrukturális különbségek a nem nociceptív szabad idegvégződések (pl. Érzékeny mechanoreceptorok és termoreceptorok) és a nociceptívek között. Funkcionálisan különböző szabad idegvégződések
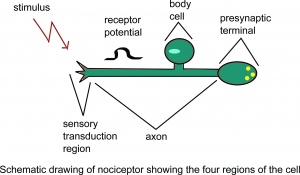
A nociceptor sematikus rajza feltételezzük, hogy a sejt négy régiója.
feltételezhető, hogy axonális membránjukban különböző receptormolekulák találhatók. Az izomnociceptorok működéséhez különösen fontos receptormolekulák savérzékelő ioncsatornák (ASIC-k), amelyek alacsony szöveti pH-n nyílnak, az adenozin-trifoszfát (ATP) és az átmeneti receptor potenciális 1. altípus (TRPV1) megkötésével aktiválódó P2X3 receptorok, amelyek érzékenyek a magas hőmérsékletre, a kapszaicin vegyi anyagra és az alacsony pH-ra. a P neuropeptid anyag rendelkezik számoltak be, hogy túlnyomórészt nociceptív afferens rostokban vannak jelen. Míg az idegrendszeren belül számos neurotranszmitter található, a nociceptív transzmisszióban a három leggyakrabban részt vevő peptid, purin és gerjesztő aminosav (EAA) található. Az EAA, különösen a glutamát, a posztszinaptikus, másodrendű neuronon váltja ki a kezdeti gerjesztő választ, majd a peptidek, beleértve a P anyagot is, felszabadulnak, ami hosszabb ideig tartó depolarizációt és tartós nociceptív transzmissziót eredményez
Nociceptorok vannak jelen sok testszövetben, de nem találtak ízületi porcban, zsigeri mellhártyában, tüdő parenchimában, szívburok, agy és zsinór szövetekben.
A nociceptorok típusai
A nociceptorokat írtak le. Néhány nociceptor reagál a káros hidegre, a káros hőre és a magas küszöbű mechanikai ingerekre, valamint a különféle kémiai mediátorokra. A nociceptorok, bár polimodálisak, a mechanikus ingerekre adott válasz alapján további két fő osztályra oszthatók, ami megkülönböztetést eredményez a mechanikailag érzékeny afferensek (MSA) és a mechanikailag érzéketlen afferensek (MIA) között, amelyeket nagyon magas mechanikai küszöbértékkel rendelkező afferensként vagy nem reagálnak a mechanikus ingerekre.
A nociceptorokat axonjaik vagy szálak átmérőjének vezetési sebessége alapján osztályozhatjuk, ez a III. és IV. csoport, illetve Aδ és C.
Közepes átmérőjű Aδ típusú mielinezett afferensek, amelyek az akut, jól lokalizált, éles szúró típusú fájdalmat közvetítik, a III. csoport afferenseként ismertek. Az Aδ afferens szálak átlagos szálátmérője 2-5 mm, vezetőképességük pedig 5-30 m / s. Az Aδ nociceptorok további két típusra oszthatók (úgy tűnik, hogy az egyes típusok körülbelül 50% -a létezik).
- Az I típusú Aδ mechanikailag érzékeny afferensek (MSA), amelyek lassan alkalmazkodó kisüléssel reagálnak az erős pontos nyomás.Hő- és kémiai ingerekre is reagálnak, és viszonylag magas hőküszöbökkel rendelkeznek (> 50C).
- A II. típusú Aδ nociceptorok hőküszöbértéke alacsonyabb, mint az I. típusú egységeké, de nagyon magas a mechanikai küszöbértékük (mechanikusan érzéketlen afferenseknek – MIA-k). Ennek az afferensnek a tevékenysége szinte biztosan közvetíti az “első” akut fájdalomreakciót a káros hő hatására. A térdízületben, a zsigerekben és a szaruhártyában számoltak be róla.
C típusú nem myelinizált afferens rostok, amelyek közvetítik rosszul lokalizált tompa, égő, úgynevezett “második” vagy lassú fájdalom a IV. csoport. Az átlagos szálátmérő 2 mm alatt van, és a vezető sebesség 2 m / s vagy kevesebb. A nem myelinizált C rostok szintén heterogének. A C rost afferensek két osztályba sorolhatók a mechanikai ingerekre adott válaszaik alapján. A mielinált Aδ afferens szálakhoz hasonlóan a legtöbb C szál polimodális, vagyis mechanikai és hőérzékeny (CMH) populációt is tartalmaz. A CMH-k reakcióját erősen befolyásolja az ingerelőzmények is. Fáradtság és szenzibilizáció egyaránt megfigyelhető. A hőre adott válasz csökkenése szintén megfigyelhető a befogadó mezőre alkalmazott mechanikai ingerek vagy az idegtörzsre alkalmazott elektromos ingerek után. Ez azt sugallja, hogy egy adott inger modalitásra adott válaszként a fáradtság heterológ ingerléssel, azaz más modalitású ingerrel történő gerjesztéssel indukálható. Ezek a domináns típusú C-rostos nociceptorok az emlősök bőrében. A mechanikailag érzéketlen C-szálak (C-MIA-k) vagy nem reagálnak a mechanikus ingerekre, vagy nagyon magas mechanikai küszöbértékkel rendelkeznek. Ezek az afferensek reagálnak a hőre és a különféle káros kémiai ingerekre (pl. Kapszaicin, hisztamin), és gyakran kemoreceptoroknak tekintik őket.
Összefoglalva a fentieket, azonnali, jól lokalizált, fukar fájdalomérzet jelentkezik. kis átmérőjű, Aδ típusú mielinált idegrostok közvetítik. A C rostok rosszul lokalizált anatómiai típusú fájdalmat közvetítenek, fájó és égő jellege van, később jelentkezik, mint a kezdeti első érzés, és nehéz megbecsülni annak erejét.
TRP csatornák
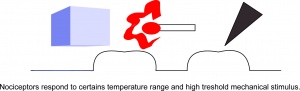
A nociceptorok reagálnak bizonyos hőmérsékleti tartományokra és mechanikai ingerekre.
Az axon perifériás vége kapszulázott fehérjéket, úgynevezett transzdukciós fehérjéket (TRP) tartalmaz, amelyeket egy adott ingerrel lehet aktiválni. A tranziens receptor potenciál (TRP) multigén szupercsalád olyan integrált membránfehérjéket kódol, amelyek ioncsatornaként működnek. A TRP csatorna család érdekes, mert több tag is érintett a nociceptor szignál transzdukciójában.
Az Aδ és C szálas nociceptorok káros hideg és káros hő ingereket detektálnak. A TRP csatornacsalád biztosítja a termikus változások detektálására alkalmas molekulák egy csoportját. Úgy tűnik, hogy az ioncsatornák aktivitása a hőmérsékletek teljes tartományát, a káros hidegtől a káros hőig terjed. A TRPM8 és a TRPV3 / 4 hűvös és meleg kódolást végez, a TRPA1 káros hideget, a TRPV1 / 2 pedig káros hőt okoz. A termoszenzitív TRP csatornák egy része kémiai és mechanikai ingerekre is reagál.
Például a TRPV1 elengedhetetlen a nociceptívum transzdukciójához a vanilloid vegyületek gyulladásos és hipotermikus hatásai révén, és hozzájárul a szöveti sérülést követő akut termikus nocicepcióhoz és termikus hiperalgéziához. A TRPV1 áramot a bradikinin és az idegnövekedési faktor számos lehetséges mechanizmus révén erősíti, és a protonok és a kapszaicin, a chili paprikában lévő „forró” vegyület is aktiválja. Az intenzív káros ingereket követő hiperalgéziával ellentétben a kapszaicin tartós expozíciója későbbi deszenzitizációt eredményezhet.
Míg a termoszenzitív TRP csatornák felfedezése nagymértékben javította a termikus ingerek transzdukciós mechanizmusainak megértését, a szelektív géndelécióval rendelkező állatok eredményei egyértelműen jelzik, hogy a termikus ingerek több és még ismeretlen transzdukciós mechanizmust is érintenek.
Kémiai mediátorok
A sérülés számos vegyi anyag helyi felszabadulását eredményezi a nem neuronális sejtekből (pl. fibroblasztok, hízósejtek, neutrofilek, monociták és vérlemezkék), valamint az elsődleges afferens rostok szenzoros termináljaiból. amelyek közvetítik vagy megkönnyítik a gyulladásos folyamatot. A gyulladásos mediátorok közé tartoznak a prosztaglandinok, a leukotriének, a bradikinin, a szerotonin, a hisztamin, az SP, a tromboxánok, a vérlemezkéket aktiváló faktor, a purinok, például az adenozin és ATP, a protonok és a szabad gyökök. A gyulladás során citokinek, például interleukinek és tumor nekrózis faktor, valamint neurotropinok, különösen NGF is keletkeznek.Érdemes megjegyezni, hogy a legtöbb ilyen vegyi anyag (főleg olyan anyagok, mint a bradikinin és a prosztaglandin E2) általában úgy vélik, hogy nem közvetlenül aktiválják a nociceptorokat, hanem inkább fokozzák a fájdalomérzetet a természetes ingerekre és más endogén vegyi anyagokra reagálva a hatás gyakoriságának növelésével. potenciális kilövés.
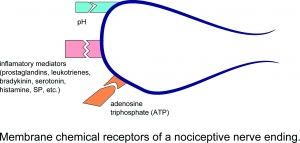
A nociceptív idegvégződés membrán kémiai receptorai.
A nociceptorok aktiválása nemcsak afferens üzeneteket továbbít a gerincvelő hátsó szarvára, hanem megindítja a neurogén gyulladás folyamatát is. A neurogén gyulladás neurotranszmitterek, nevezetesen a P anyag és a kalcitonin génnel kapcsolatos peptid (CGRP) felszabadulását idézi elő, ami súlyos értágulathoz vezet, valamint fehérje és folyadék szivárgásához vezet a kapilláris utáni vénákból.
Két vegyi anyag különösen érdekes:
- Adenozin-trifoszfát (ATP)
Az ATP az energiát hordozó molekula a test minden sejtjében. Trauma és egyéb kóros elváltozások során minden szövetből felszabadul, amelyek a sejthalállal járnak. Emiatt az ATP-t a szöveti traumák és fájdalmak általános jelzőanyagának tekintették. Humán mikroneurográfiai vizsgálatokban az ATP injekciója aktiválta a mechano-érzékeny és mechano-érzéketlen C-nociceptív rostok 60% -át anélkül, hogy ezeket a rostokat mechanikus vagy hőingerekre érzékenyítené. Az ATP aktiválja a purinerg P2X3 receptorokat a nociceptorokban, ami kisülést okoz. Az ATP különösen fontos izomfájdalom esetén, mert nagy koncentrációban van jelen az izomsejtekben.
- A szövetek pH-jában bekövetkező protonváltozás
A savérzékelő ioncsatornák (ASIC-k) olyan receptormolekulák családját alkotják, amelyek érzékenyek a pH-csökkenésre és nyitottak különböző pH-értékeken. A csatornafehérjék már túl kicsi pH-változásokra reagálnak. Ez a receptorcsalád (például ASIC1 és ASIC3) különösen fontos az izomfájdalom szempontjából, mivel az izom szinte minden kóros elváltozását a szövetek pH-értékének csökkenése kíséri, például kimerítő testmozgás, ischaemia és a megerősítés.
A nociceptorok elhelyezkedése
A nociceptorok sejtteste a periféria hátsó gyökér ganglionjában (DRG) és az arc trigeminus ganglionjában található. Axonjaik a perifériás idegrendszerbe nyúlnak, és fogékony mezőket létrehozó ágakban végződnek.
- Bőr
A bőrben végződő szabad idegvégződések jelentik a helyi mechanikai, termikus és kémiai változások jelzésének mechanizmusát. A bőr szabad idegvégződéseinek nagy többségét polimodális nociceptoroknak nevezzük, mivel több receptort tartalmaznak, és így reagálnak a fent említett inger különböző kombinációira. Az I típusú Aδ magas küszöbű mechanoreceptor egységek sűrűn oszlanak el a szőrös és ropogós bőrben.
- Izmok
Receptormolekulák, amelyek különösen fontosak a Az izom nociceptorok funkciója az alacsony szöveti pH-n megnyíló savérzékelő ioncsatornák (ASIC), az adenozin-trifoszfát (ATP) megkötésével aktiválódó P2X3 receptorok és a magas érzékenységre érzékeny tranziens receptor-1-es receptor (TRPV1) hőmérséklet és alacsony pH.
A vázizomzatban a szabad idegvégződések meglehetősen egyenletesen oszlanak meg. Nem találtunk különbséget a patkány gastrocnemius – soleus izom proximális és distalis része között. Ugyanebben a vizsgálatban azonban a patkány calcanealis ín peritendineumában az ideggyűrű sűrűségét többszörösen nagyobbnak találták, mint a GS izomban. Ezzel szemben a saját ínszövet kollagén nyalábkötegeiben szinte mentesek voltak szabad idegvégződések. a környező izmok idegei és a bőr idegéből származó kis fasciculusok biztosítják, de ez magában foglalja az összes idegvégződést. A szabad idegvégződések az inak belsejében vannak ábrázolva, de főként a peritendinous szövetekben vannak fájdalomreceptorok. Az összes idegrost és idegvégződés száma és elhelyezkedése az ín funkciójától függően változik, jobban látható a finom mozgásokban részt vevő kisebb inakban.
- Ízület
Az ízületekben a nociceptorok az ízületi tokban, az ínszalagokban és a proximális inakban, a csontban, a periosteumban, az ízületi zsírpárnában és az erek körül helyezkednek el, de nem az ízületi porcban. A magas küszöbű nociceptív afferensek elsősorban a szinoviumban és a periosteumban végződnek, és általában csak az ízület mozgási határán túli mozgására reagálnak. Az ízületi károsodást követően két tényező együttesen változtatja meg az ízületi nociceptorok mechanikai érzékenységét.Először a fizikai változások (ízületi effúzió és szöveti ödéma) megváltoztatják az ízületi szövetekre gyakorolt nyugalmi és mozgás által kiváltott erőket, másodszor pedig a sérült szövetben felszabaduló fl gyulladásos mediátorokban az idegvégződések receptoraihoz kötődve érzékenyítik az ízületi nociceptív afferenseket. Az ízület sok nociceptora reagál az ártalmatlan mozgásokra, de egyre inkább aktiválódnak, ha a mozgások meghaladják a fiziológiai munkaterületet, míg más nociceptorok kizárólag a káros mozgások alatt aktívak. Az úgynevezett néma nociceptorok harmadik csoportja általában inaktív és csak kóros körülmények között reagál, például fl ammáció esetén.
Kimutatták, hogy az ágyéki ágyéki ízületi kapszulát a nociceptorok és a proprioceptív rostok gazdagon beidegzik. Normál állapotban az olyan nociceptorok, mint amelyek a facet ízületi kapszulában láthatók, magas küszöbértékkel rendelkeznek, és nem várható, hogy kisülnének, hacsak a terhelés nem szuprafiziológiai. Kóros ízületi gyulladás jelenlétében azonban a synovitis kémiai mediátorai szenzibilizálhatják ezeket a nociceptorokat, és a fájdalom stimulálásához már nem szükséges a szupraphysiológiai stresszszint. Ilyen gyulladásos mediátorokat (P anyag, bradikinin, foszfolipáz A2) észleltek a facet ízületi kapszulában.
A csigolyaközi lemezekben található nociceptorok általában a gyűrű külső részére korlátozódnak. diszkogén fájdalom esetén, amikor a nagyobb gyűrűs területen kiterjednek, és az ér és a rögzítések mentén tovább hatolnak a degenerált korongba. Valószínűleg ezek a C- és A δ-kötők felelősek a fájdalomreakciók továbbításáért. A csigolyaközi porckorong hátsó hosszanti szalagja és a külső gyűrűs fi brusus rétegei rengeteg nociceptív kötést tartalmaznak. Idegszálak és idegvégződések a zygapophysialis ízületek subchondralis csontjában is előfordulnak. A subchondralis csonttól az ízületi porcig terjedő eróziós csatornákban fordulnak elő.
Egy ember által végzett tanulmány (Kiter et al., 2010) mind a szabad, mind a beágyazott idegvégződéseket kimutatta az emberi iliolumbalis szalagon. Studie (Hirsch és mtsai., 1963) felvetette, hogy a supraspinous és intraspinous szalagokban finom idegtöltők és komplex kapszulázatlan végek találhatók.
- Viscera
A zsigeri nociceptorok nem reagálnak olyan vágási vagy égési sérülésekre, mint a perifériás bőrszövetben lévő társaik. Ehelyett a kóros változásra reagálva aktiválódnak. Fájdalmat okozó ingerek a zsigerekben, beleértve a tapadást a bélfenéken, gyulladás, az üreges izomfalú szervek, például a gyomor-bélrendszer, a húgyúti, az epehólyag megnyúlása és az ilyen üreges szerveket körülvevő izomrétegek erős összehúzódása, vegyi anyagokat irritáló anyagok vagy ischaemia olyan szervekben, mint szív. Ezeknek a láncszemeknek az eloszlása a szervek között változó. A magas küszöbértékű receptorok kizárólag azokat a szerveket innerválják, amelyekből a fájdalom az egyetlen tudatos érzés (azaz ureter, vese, tüdő, szív), de viszonylag kevés olyan szervben, amely ártalmatlan és káros érzéseket okoz (pl. Vastagbél, gyomor és hólyag), főleg alacsony küszöbű receptorok innerválják. Az olyan szerveknek, mint a máj, a tüdő, a vesék és a hasnyálmirigy, kevés receptoruk van, de ezekből a szervekből származó fájdalom leginkább e szervek kapszuláiban lévő receptorok aktiválásából származik. A zsigerek nociceptív stimulálása diffúz fájdalomhoz vezet, amelyet nehéz lokalizálni. A zsigerek afferens nociceptív rostjai a szimpatikus és a paraszimpatikus idegekkel együtt találhatók. A zsigeri szervek többségét a vagális ideg innerválja, de a vizsgálatok nem mutatják egyértelműen, hogy ez az ideg képes-e hordozni nociceptív afferens bemenetet. Egyes tanulmányok azonban egyértelműen bizonyítják, hogy a vagális afferensek a nagy intenzitású mechanikai ingerekről adnak információt a központi idegrendszerbe. Számos ember vagy állat bevonásával végzett vizsgálat kimutatta, hogy a gerincvelő elváltozású alanyok képesek jelenteni a valószínűleg a zsigeri szervek területéről származó fájdalmat.
- 1.0 1.1 Loeser JD, Treede RD. Az IASP Basic Pain Terminology kiotói protokollja. Fájdalom. 2008; 137 (3): 473–7. doi: 10.1016 / j.pain.2008.04.025. PMID 18583048
- Basbaum AI, Jessell T. A fájdalom érzékelése. In: Kandel ER, Schwartz J, Jessell T. szerkesztők. Az idegtudomány alapelvei. New York: Appleton és Lange; 2000. p472-491. P.
- 3,0 3,1 3,2 3,3 3,4 3,5 3,5 Meyer RA, Ringkamp M, Campbell JN, Raja SN. A bőr nocicepciójának perifériás mechanizmusai. In: McMahon SB, Koltzenburg M, szerkesztők. Wall és Melzack fájdalomtankönyve. London: Elsevier; 2006. p3–34.
- Lloyd DPC. A macska ipsilaterális hátsó végtag reflexeinek átvitelét szabályozó neuronminták. J Neurophysiol. 1943; 6: 293–315
- 5,0 5,1 5,2 5 Schaible HG, Schmidt RF. Egy kísérleti ízületi gyulladás hatása a finom ízületi afferens egységek szenzoros tulajdonságaira. Journal of Neurophysiology. 1985; 54: 1109-1122
- Häbler HJ, Jänig W, Koltzenburg M.Új típusú nem myelinizált kemoszenzitív nociceptor az akut gyulladású húgyhólyagban. Ügynökök és cselekvések. 1988; 25: 219-221.
- Taneliai DL. A szaruhártya afferens idegek populációjának kolinerg aktiválása. Kísérleti agykutatás. 1991; 86: 414-420
- LaMotte RH, Campbell JN. Majomban a meleg és nociceptív C-rost afferensek reakcióinak összehasonlítása a hőfájdalom emberi megítélésével. Journal of Neurophysiology. 1978; 41: 509-528.
- Treede RD, Meyer RA, Raja SN, Campbell JN. Bizonyíték két különböző hőátadási mechanizmusról a majom bőrét innerváló nociceptív primer afferensekben Élettani Közlöny. 1995; 483: 747-758
- Schepers RJ, Ringkamp M. termoreceptorok és hőérzékeny afferensek. Idegtudomány & Biobevavioral Reviews. 2010; 34 (2): 177-184
- Caterina MJ, Schumacher MA, Tominaga M, Rosen TA, Levine JD, Julius D. A kapszaicin receptor: hő által aktivált ioncsatorna a fájdalom útjában. Nature 1997; 389: 816–824
- Bjur D, Alfredson H, Forsgren S. Az emberi Achilles-ín beidegződési mintázata: a normál és az ín-ín vizsgálata az általános és az érzékszervi beidegzés markereivel. Sejtszövet Res. 2005; 320: 201-206
- 13,0 13,1 Ashton IK, Ashton BA, Gibson SJ, Polak JM, Jaffray DC, Eisenstein SM. A hátfájás morfológiai alapjai: idegtöltők és neuropeptidek bemutatása az ágyéki facet ízületi kapszulában, de a ligamentum um avum-ban nem. J Orthop Res. 1992; 10 (1): 72-78
- Kiter E, Karaboyun T, Tufan AC, Acar K. ImmunohistochemicalfckLR szabad idegvégződések bemutatása az iliolumbalis szalagon. Gerinc. 2010; 35 (4): E101-4. doi: 10.1097 / BRS.0b013e3181ae561d.
- Hirsch C, Ingelmark BE, Miller M. A lowfckLRback fájdalom anatómiai alapjai. Szenzoros idegvégződések jelenlétének vizsgálata infckLRligamentos, kapszuláris és csigolyaközi porckorongszerkezetek a thefckLRhuman ágyéki gerincben. Acta Orthop Scand. 1963; 33: 1–17.
- Moller, Aage (2014-04-22). Fájdalom, anatómiája, élettana és kezelése. Kindle Edition.
