Nociceptorer kan aktiveras av tre typer av stimulans inom målvävnaden – temperatur (termisk), mekanisk (t.ex. stretch / töjning) och kemisk (t.ex. pH-förändring som ett resultat av lokal inflammatorisk process). Således kan en skadlig stimulans kategoriseras i en av dessa tre grupper.
Termerna nociception och smärta bör inte användas synonymt, eftersom var och en kan förekomma utan den andra .. Smärta som uppstår vid aktivering av nociceptorerna kallas nociceptiv smärta. Nociceptiv smärta kan klassificeras enligt den vävnad där nociceptoraktivering inträffade: ytlig somatisk (t.ex. hud), djup somatisk (t.ex. ligament / senor / ben / muskler) eller visceral (inre organ).
Nociception pathway
Inte alla nociceptorer svarar på varje typ av skadliga stimuli. Den uppenbara avsaknaden av ett svar på en skadlig stimulans kan orsakas på grund av olika receptorer placerade på ändterminalens membran (fri nervänd) eller stimulusintensiteten är otillräcklig. Vanligtvis är stimuleringströskeln för en nociceptor under vävnadsskadande intensitet. Nociceptorer har heterogena egenskaper, som svarar på multipla stimuleringsmodaliteter (polymodal). Emellertid kan tillämpningen av skadlig stimulans av en modalitet förändra svarsegenskaperna hos nociceptorn till andra modaliteter. Tillämpningen av en viss stimulans under en given tidsperiod kan också inducera långvariga förändringar i nociceptorns svarsegenskaper. Skada och skada minskar tröskeln och ökar responsens storlek för en given stimulans, ett fenomen som kallas perifer sensibilisering. Av särskilt intresse är värmeavgivande men mekaniskt okänsliga omyeliniserade afferenter som utvecklar mekanisk känslighet endast i samband med skada.
Nociceptorer har det morfologiska utseendet på fria nervändar. Uttrycket ”fri nervändning” indikerar att i ljusmikroskopet ingen (korpuskulär) mottaglig struktur kan kännas igen. För närvarande finns det inga tydliga ultrastrukturella skillnader mellan icke-nociceptiva fria nervändar (t.ex. känsliga mekanoreceptorer och termoreceptorer) och nociceptiva sådana Funktionellt, olika fria nervändar
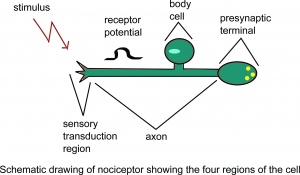
Schematisk ritning av nociceptor som visar fyra regioner i cellen.
antas ha olika uppsättningar receptormolekyler i sitt axonala membran. Receptormolekyler som är särskilt viktiga för muskelnociceptors funktion är syrakänsliga jonkanaler (ASIC) som öppnas vid lågt vävnads-pH, P2X3-receptorer som aktiveras genom bindning av adenosintrifosfat (ATP) och den transienta receptorpotentialreceptorsubtyp 1 (TRPV1) som är känslig för höga temperaturer, capsaicinkemikalier och lågt pH. neuropeptidsubstans P har har rapporterats vara huvudsakligen närvarande i nociceptiva afferenta fibrer. Medan det finns många neurotransmittorer i nervsystemet är de tre vanligaste som deltar i nociceptiv överföring peptider, puriner och excitatoriska aminosyror (EAA). EAA, särskilt glutamat, producerar det initiala excitatoriska svaret på det postsynaptiska, andra ordningens neuron, följt av frisättning av peptider, inklusive substans P, vilket orsakar en mer långvarig depolarisering och ihållande nociceptiv överföring
Nociceptorer är närvarande i många kroppsvävnader men har inte hittats i ledbrosk, visceral pleura, lungparenkym, perikardium, hjärna och sladdvävnad.
Typer av nociceptorer
Flera klasser av nociceptorer har beskrivits. Vissa nociceptorer svarar på skadlig förkylning, skadlig värme och mekaniska stimuli med hög tröskel samt en mängd olika kemiska medlare. Nociceptorer, även om de är polymodala, kan delas vidare i två huvudklasser på grundval av svar på mekaniska stimuli, vilket leder till en skillnad mellan mekaniskt känsliga afferenter (MSA) och mekaniskt okänsliga afferenter (MIA) definierade som afferenter som har mycket höga mekaniska trösklar eller inte svarar på mekaniska stimuli.
Nociceptorer kan klassificeras efter ledningshastigheten för deras axoner eller fibrernas diameter, detta är grupp III respektive IV ord Aδ respektive C.
Typ Aδ myeliniserade afferenter med medium diameter som förmedlar akut, väl lokaliserad, skarp stickande smärta, känd som grupp III afferent. Aδ-afferenta fibrer har genomsnittlig fiberdiameter 2-5 mm och ledande hastighet 5-30 m / s. Aδ-nociceptorer kan ytterligare delas in i två typer (det verkar finnas ungefär 50% av varje typ)
- Typ I Aδ är mekaniskt känsliga afferenter (MSA) som svarar med en långsamt anpassande urladdning till stark punkttryck.De svarar också på värme och kemiska stimuli och har relativt höga värmetrösklar (> 50C).
- Nuciceptorer av typ II Aδ har lägre värmetröskel än typ I-enheter men har mycket höga mekaniska trösklar (kallas mekaniskt okänsliga afferenter – MIA). Denna afferents aktivitet förmedlar nästan säkert det ”första” akuta smärtsvaret mot skadlig värme. De har rapporterats i knäleden, inälvorna och hornhinnan.
Typ C omyeliniserade afferenta fibrer som förmedlar dåligt lokaliserad tråkig, brännande, så kallad ”andra” eller långsam smärta kallas grupp IV. Den genomsnittliga fiberdiametern är under 2 mm och den ledande hastigheten är 2 m / s eller mindre. De omyeliniserade C-fibrerna är också heterogena. C-fiberavledare kan delas in i två klasser baserat på deras svar på mekaniska stimuli. Liksom de myeliniserade Aδ-afferenta fibrerna är de flesta C-fibrer polymodala, det vill säga de inkluderar en population som är både mekaniskt och värmekänslig (CMH). Responsen från CMH påverkas också starkt av stimulushistoriken. Både trötthet och sensibilisering observeras. En minskning av svaret på värme observeras också efter mekaniska stimuli applicerade på det mottagliga fältet eller elektriska stimuli som appliceras på nervstammen. Detta antyder att utmattning som svar på en given stimulusmodalitet kan induceras av heterolog stimulering, det vill säga genom excitation med en stimulans av en annan modalitet. Dessa är den dominerande typen av C-fiber-nociceptorer i däggdjurshud. Mekaniskt okänsliga C-fibrer (C-MIA) svarar antingen på mekaniska stimuli eller har en mycket hög mekanisk tröskel. Dessa afferenter svarar på värme och olika skadliga kemiska stimuli (t.ex. capsaicin, histamin) och anses ofta vara kemoreceptorer.
Sammanfattningsvis till ovanstående är omedelbar, väl lokaliserad, snål smärtsensation medierad av myeliniserade nervfibrer med liten diameter, typ Aδ. C-fibrer förmedlar dåligt lokaliserad anatomiskt typ av smärta, den har värkande och brännande karaktär, kommer senare än den första första känslan och det är svårt att uppskatta dess styrka.
TRP-kanaler
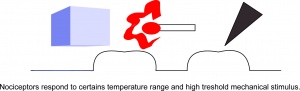
Nociceptorer svarar på ett visst temperaturintervall och mekanisk stimulans.
Axonens perifera ände innehåller inkapslade proteiner som kallas transduktionsproteiner (TRP), som kan aktiveras av en specifik stimulans. Den transienta receptorpotentialen (TRP) multigen superfamilj kodar integrerade membranproteiner som fungerar som jonkanaler. TRP-kanalfamiljen är av intresse eftersom flera medlemmar har varit inblandade i transduktion av nociceptorsignaler.
Skadlig kyla och skadlig värmestimuli detekteras av Aδ- och C-fibernociceptorer. TRP-kanalfamiljen tillhandahåller en grupp molekyler utrustade för att detektera termiska förändringar. Hela temperaturområdet, från skadlig kyla till skadlig värme, verkar omvandlas av aktiviteten i dessa jonkanaler. TRPM8 och TRPV3 / 4 kodar för sval och varm respektive, TRPA1 överför skadlig kyla och TRPV1 / 2 avkänner skadlig värme. Några av de termokänsliga TRP-kanalerna svarar också på kemiska och mekaniska stimuli.
Till exempel är TRPV1 viktigt för att transducera nociceptiva genom inflammatoriska och hypotermiska effekter av vanilloidföreningar och bidrar till akut termisk nociception och termisk hyperalgesi efter vävnadsskada. TRPV1-ström förstärks av bradykinin och nervtillväxtfaktor via flera möjliga mekanismer och aktiveras också av protoner och capsaicin, den ”” heta ”föreningen i chilipeppar. I motsats till hyperalgesi efter intensiva skadliga stimuli, kan långvarig exponering för capsaicin resultera i efterföljande desensibilisering.
Även om upptäckten av termokänsliga TRP-kanaler har förbättrat vår förståelse av transduktionsmekanismer för termiska stimuli, har fynd hos djur med selektiv genradering klart indikerar att flera och ännu okända transduktionsmekanismer är engagerade av termiska stimuli.
Kemiska medlare
Skador resulterar i lokal frisättning av många kemikalier från icke-neuronala celler (t.ex. fibroblaster, mastceller, neutrofiler, monocyter och trombocyter), samt från sensoriska terminaler av primära afferenta fibrer som förmedlar eller underlättar den inflammatoriska processen. Inflammatoriska mediatorer inkluderar prostaglandiner, leukotriener, bradykinin, serotonin, histamin, SP, tromboxaner, trombocytaktiverande faktor, puriner såsom adenosin och ATP, protoner och fria radikaler. Cytokiner, såsom interleukiner och tumörnekrosfaktor, och neurotrofiner, särskilt NGF, genereras också under inflammation.Det är värt att notera att de flesta av dessa kemikalier (främst ämnen som bradykinin och prostaglandin E2) allmänt anses inte aktivera nociceptorer direkt utan förstärker känslan av smärta som svar på naturliga stimuli och andra endogena kemikalier genom att öka verkningsfrekvensen potentiell avfyrning.
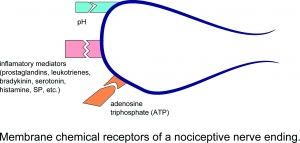
Membrankemiska receptorer för en nociceptiv nervänd.
Aktivering av nociceptorer överför inte bara afferenta meddelanden till ryggmärgs dorsala horn utan initierar också processen med neurogen inflammation. Neurogen inflammation orsakar frisättning av neurotransmittorer, särskilt substans P och kalcitoningen-relaterad peptid (CGRP), vilket leder till svår vasodilatation, samt plasmaläckage av proteiner och vätska från postkapillärvenuler.
Två kemikalier är av särskilt intresse:
- Adenosintrifosfat (ATP)
ATP är den energibärande molekylen i alla kroppens celler. Det frigörs från alla vävnader under trauma och andra patologiska förändringar som är associerade med celldöd. Av denna anledning har ATP ansetts vara en allmän signalsubstans för vävnadsskada och smärta. I mänskliga mikronurografiska studier aktiverade injektion av ATP 60% av mechano-responsiva och mechano-okänsliga C-nociceptiva fibrer utan att sensibilisera dessa fibrer för mekaniska eller värmestimuli. ATP aktiverar purinerga P2X3-receptorer i nociceptorer som orsakar urladdning. ATP är särskilt viktigt för muskelsmärta eftersom det finns i muskelceller i hög koncentration.
- Protoner förändring i vävnads pH
Syrakänsliga jonkanaler (ASIC) utgör en familj av receptormolekyler som är känsliga för ett pH-fall och öppna vid olika pH-värden. Kanalproteinerna reagerar redan för små pH-förändringar. Denna receptorfamilj (till exempel ASIC1 och ASIC3) är särskilt viktig för muskelsmärta, eftersom nästan alla patologiska förändringar i muskler åtföljs av en minskning i vävnads pH, t.ex. utmattande träning, ischemi och skymning.
Plats för nociceptorer
Nociceptors cellkroppar är belägna i ryggganglierna (DRG) för periferin och trigeminal ganglion för ansiktet. Deras axoner sträcker sig in i det perifera nervsystemet och slutar i grenar och skapar mottagliga fält.
- Hud
Fria nervändar som slutar i huden är maskinerna för att signalera lokala mekaniska, termiska och kemiska förändringar. Den stora majoriteten av fria nervändar i huden kallas polymodala nociceptorer eftersom de innehåller flera receptorer och således svarar på olika kombinationer av ovan nämnda stimulus. Typ I Aδ-mekanismer med hög tröskelvärden är tätt fördelade i hårig och glättig hud.
- Muskler
Receptormolekyler som är särskilt viktiga för muskelnociceptors funktion är syrakännande jonkanaler (ASIC) som öppnas vid lågt vävnads-pH, P2X3-receptorer som aktiveras genom bindning av adenosintrifosfat (ATP) och den transienta receptorpotentialreceptorsubtyp 1 (TRPV1) som är känslig för hög temperaturer och lågt pH.
I skelettmuskeln verkar de fria nervändarna fördelas ganska jämnt. Ingen skillnad mellan de proximala och distala delarna av råtta gastrocnemius – soleus muskel hittades. I samma studie befanns dock nervfibertätheten i peritendineum hos råttkalkaneal sena vara flera gånger högre än i GS-muskeln. Däremot var kollagenfibersamlingarna i själva senvävnaden nästan fria från fria nervändar.
- Senor
Innervation av Achilles senor människa tillhandahålls av nerver från de omgivande musklerna och av små fasciculi från kutana nerver men detta involverar all nervändning. Fria nervändar är representerade inuti senorna, men huvudsakligen i peritendinös vävnad är smärtreceptorer. Antalet och platsen för alla nervfibrer och nervändar varierar beroende på senans funktion, eftersom de är mer representerade i de mindre senorna som är involverade i fina rörelser.
- Led
Nociceptorer i lederna finns i ledkapseln, ligament och proximala senor, ben, periosteum, ledfettplatta och runt blodkärlen men inte i ledbrosket. Nociceptiva afferenter med hög tröskel avslutas främst i synovium och periosteum och svarar normalt bara på ledens rörelse utanför arbetsgränserna. Efter ledskador kombineras två faktorer för att förändra den mekaniska känsligheten hos artikulära nociceptorer.För det första förändrar fysiska förändringar (ledutgjutning och vävnadsödem) de vilande och rörelseinducerade krafter som utövas på ledvävnaderna, och för det andra sensibiliserar ammatoriska mediatorer som släpps in i den skadade vävnaden artikulära nociceptiva afferenter genom att binda till receptorer på nervändarna. Många nociceptorer i leden svarar på oskadliga rörelser men aktiveras alltmer när rörelser överskrider det fysiologiska arbetsområdet, medan andra nociceptorer är aktiva uteslutande under skadliga rörelser. Den tredje gruppen av så kallade tysta nociceptorer är normalt inaktiva och svarar endast under patologiska omständigheter som vid skymning.
Ländryggsfogens kapsel har visat sig vara rikt innerverad av nociceptorer och proprioceptiva fibrer. I ett normalt tillstånd har nociceptorer som de som ses i fasettledskapseln en hög tröskel och förväntas inte släppas ut om inte belastningar är suprafysiologiska. I närvaro av patologisk ledinflammation kan emellertid kemiska medlare för synovit sensibilisera dessa nociceptorer och suprafysiologiska nivåer av stress kanske inte längre krävs för att stimulera smärta. Sådana inflammatoriska mediatorer (substans P, bradykinin, fosfolipas A2) har detekterats i facettledskapseln.
Nociceptorer i intervertebrala skivor är normalt begränsade till den yttre tredjedelen av ringen, kan vara substratet för diskogen smärta när de expanderas över det större ringformiga området och tränger vidare in i den degenererade skivan längs kärlsystemet och fi surerna. Dessa C- och A δ-fibrer är sannolikt ansvariga för att överföra smärtsvar. Det bakre längsgående ligamentet och de yttre ringformade fi brosus-lagren på intervertebral skiva innehåller massor av nociceptiva fibrer. Nervfibrer och nervändar förekommer också i det subkondrala benet i de zygapofysiala lederna. De förekommer i erosionskanaler som sträcker sig från det subkondrala benet till ledbrosket.
En mänsklig studie av (Kiter et al., 2010) visade både fria och inkapslade nervändar i det mänskliga iliolumbar ligamentet. Studie av (Hirsch et al., 1963) föreslog förekomsten av fin nervfibrer och komplexa oinkapslade ändar i de supraspinösa och intraspinösa ligamenten.
- Viscera
Viscerala nociceptorer svarar inte på skär- eller brännskador som deras motsvarigheter i perifer kutan vävnad. Istället aktiveras de som svar på patologisk förändring. Smärtproducerande stimuli i inälvorna inklusive traktion på mesenteriet, inflammation, utspänning av ihåliga muskelväggiga organ som mag-tarmkanalen, urinvägarna, gallblåsan och starka sammandragningar av muskelskikt som omger sådana ihåliga organ, kemikalier irriterande eller ischemi i organ som t.ex. hjärta. Fördelningen av dessa fibrer varierar mellan organen. Högtröskelreceptorer uteslutande innerverade organ från vilka smärta är den enda medvetna känslan (dvs. urinledare, njure, lungor, hjärta), men är relativt få i organ som ger oskadliga och skadliga känslor (t.ex. kolon, mage och urinblåsa), innerveras mestadels av lågtröskelreceptorer. Organ, såsom lever, lungor, njurar och bukspottkörteln, har få receptorer, men smärtan från dessa organ kommer mestadels från aktivering av receptorer i kapslarna i dessa organ. Nociceptiv stimulering av inälvor leder till diffus smärta som är svår att lokalisera. Afferenta nociceptiva fibrer i inälvor finns i samband med sympatiska och parasympatiska nerver. Majoriteten av viscerala organ är innerverade av vaginal nerv, men studier visar inte tydligt huruvida denna nerv kan bära nociceptiv afferent input. Vissa studier visar dock tydligt att vagala afferenter förmedlar information om mekaniska stimuli med hög intensitet till centrala nervsystemet. Ett antal studier som involverade människor eller djur har visat att personer med ryggmärgsskada kan rapportera smärta som troligen härrör från området med inre organ.
- 1.0 1.1 Loeser JD, Treede RD. Kyotoprotokollet enligt IASP Basic Pain Terminology. Smärta. 2008; 137 (3): 473–7. doi: 10.1016 / j.pain.2008.04.025. PMID 18583048
- Basbaum AI, Jessell T. Perception of Pain. I: Kandel ER, Schwartz J, Jessell T. redaktörer. Principer för neurovetenskap. New York: Appleton och Lange; 2000. s472-491
- 3.0 3.1 3.2 3.3 3.4 3.5 Meyer RA, Ringkamp M, Campbell JN, Raja SN. Perifera mekanismer för kutan nociception. I: McMahon SB, Koltzenburg M, redaktörer. Wall and Melzacks Textbook of Pain. London: Elsevier; 2006. s3–34.
- Lloyd DPC. Neuronmönster som styr överföring av ipsilaterala bakbenreflexer hos katt. J Neurophysiol. 1943; 6: 293–315
- 5,0 5,1 5,2 5,2 Schaible HG, Schmidt RF. Effekter av en experimentell artrit på de sensoriska egenskaperna hos fina artikulära afferenta enheter. Journal of Neurophysiology. 1985; 54: 1109-1122
- Häbler HJ, Jänig W, Koltzenburg M.En ny typ av omyeliniserad kemosensitiv nociceptor i den akut inflammerade urinblåsan. Agenter och åtgärder. 1988; 25: 219-221
- Tanelian DL. Kolinerg aktivering av en population av hornhinnans afferenta nerver. Experimentell hjärnforskning. 1991; 86: 414-420
- LaMotte RH, Campbell JN. Jämförelse av svar från varma och nociceptiva afferenter av C-fiber hos apa med mänskliga bedömningar av termisk smärta. Journal of Neurophysiology. 1978; 41: 509-528
- Treede RD, Meyer RA, Raja SN, Campbell JN. Bevis för två olika värmetransduktionsmekanismer i nociceptiva primära afferenter som innerverar apahud. Journal of Physiology. 1995; 483: 747-758
- Schepers RJ, Ringkamp M. Thermoreceptors and thermosensitive afferents. Neurovetenskap & Biobeteende. 2010; 34 (2): 177-184
- Caterina MJ, Schumacher MA, Tominaga M, Rosen TA, Levine JD, Julius D. Capsaicinreceptorn: en värmeaktiverad jonkanal i smärtvägen. Natur 1997; 389: 816–824
- Bjur D, Alfredson H, Forsgren S. Innerveringsmönstret för den mänskliga Achilles senan: studier av den normala och tendinos senan med markörer för allmän och sensorisk innervation. Cellvävnad Res. 2005; 320: 201-206
- 13.0 13.1 Ashton IK, Ashton BA, Gibson SJ, Polak JM, Jaffray DC, Eisenstein SM. Morfologisk grund för ryggsmärta: demonstration av nervfibrer och neuropeptider i ländryggsfogens kapsel men inte i ligamentum fl avum. J Orthop Res. 1992; 10 (1): 72-78
- Kiter E, Karaboyun T, Tufan AC, Acar K. ImmunohistochemicalfckLRdemonstration av fria nervändar i iliolumbar ligament. Ryggrad. 2010; 35 (4): E101-4. doi: 10.1097 / BRS.0b013e3181ae561d.
- Hirsch C, Ingelmark BE, Miller M. Den anatomiska grunden för smärta i lågfckLRback. Studier av närvaron av sensoriska nervändar infckLRligamentösa, kapsulära och intervertebrala skivstrukturer i fckLRhuman ländryggen. Acta Orthop Scand. 1963; 33: 1–17.
- Moller, Aage (2014-04-22). Smärta, dess anatomi, fysiologi och behandling. Kindle Edition.
