Nociceptorer kan aktiveres av tre typer stimulans i målvevet – temperatur (termisk), mekanisk (f.eks. Strekk / belastning) og kjemisk (f.eks. PH-endring som et resultat av lokal inflammatorisk prosess). Dermed kan en skadelig stimulans kategoriseres i en av disse tre gruppene.
Begrepene nociception og smerte skal ikke brukes synonymt, fordi hver kan oppstå uten den andre .. Smerter som oppstår ved aktivering av nociceptorene kalles nociceptive smerte. Nociceptive smerter kan klassifiseres i henhold til vevet der nociceptoraktivering skjedde: overfladisk somatisk (f.eks. Hud), dyp somatisk (f.eks. Leddbånd / sener / bein / muskler) eller visceral (indre organer).
Nociception pathway
Ikke alle nociceptorer svarer på hver type av skadelige stimuli. Den tilsynelatende mangelen på respons på en skadelig stimulus kan oppstå på grunn av forskjellige reseptorer plassert på endeterminalens membran (fri nerveende) eller stimulusintensiteten er utilstrekkelig. Vanligvis er stimuleringsterskelen til en nociceptor under vevskadelig intensitet. Nociceptorer har heterogene egenskaper, som reagerer på flere stimuleringsmodaliteter (polymodal). Imidlertid kan anvendelsen av skadelig stimulus av en modalitet endre responsegenskapene til nociceptoren til andre modaliteter. Anvendelsen av en bestemt stimulus i en gitt tidsperiode kan også indusere langsiktige endringer i responsegenskapene til nociceptoren. Skader og skader reduserer terskelen og øker responsens størrelse for en gitt stimulans, et fenomen kjent som perifer sensibilisering. Av spesiell interesse er de varmefølsomme, men mekanisk ufølsomme, ikke-myeliniserte afferenter som bare utvikler mekanisk følsomhet i skader.
Nociceptorer har det morfologiske utseendet på frie nerveender. Uttrykket «fri nerveavslutning» indikerer at det i lysmikroskopet ikke er noen (korpuskulær) mottakelig struktur som kan gjenkjennes. For tiden er det ingen klare ultrastrukturelle forskjeller mellom ikke-nociceptive frie nerveender (f.eks. Sensitive mekaniske reseptorer og termoreseptorer) og nociceptive. Funksjonelt, forskjellige frie nerveender
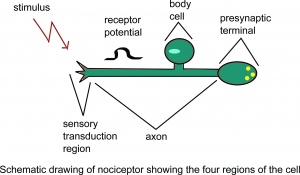
Skjematisk tegning av nociceptor som viser fire regioner i cellen.
antas å ha forskjellige sett med reseptormolekyler i sin aksonale membran. Reseptormolekyler som er spesielt viktige for funksjonen til muskelnociceptorer er syrefølende ionekanaler (ASIC) som åpnes ved lavt vevs-pH, P2X3-reseptorer som aktiveres ved binding av adenosintrifosfat (ATP), og den forbigående reseptorpotensialreseptorundertype 1 (TRPV1) som er følsom for høye temperaturer, capsaicin-kjemikalier og lav pH. nevropeptidsubstans P har blitt rapportert å være tilstede hovedsakelig i nociceptive afferente fibre. Mens det er mange nevrotransmittere i nervesystemet, er de tre vanligste som deltar i nociceptiv overføring peptider, puriner og eksitatoriske aminosyrer (EAA). EAA, spesielt glutamat, produserer den opprinnelige eksitatoriske responsen på postsynaptisk, andre ordens, neuron, etterfulgt av frigjøring av peptider, inkludert substans P, forårsaker en mer langvarig depolarisering og vedvarende nociceptiv overføring
Nociceptors er til stede i mange kroppsvev, men har ikke blitt funnet i leddbrusk, visceral pleura, lungeparenkym, perikardium, hjerne og ledningsvev.
Typer nociceptorer
Flere klasser av nociceptorer er beskrevet. Noen nociceptorer reagerer på skadelig kulde, skadelig varme og mekaniske stimuli med høy terskel, samt en rekke kjemiske mediatorer. Selv om polymodale, kan nociceptorer deles inn i to hovedklasser på grunnlag av respons på mekaniske stimuli, noe som fører til et skille mellom mekanisk følsomme afferenter (MSA) og mekanisk ufølsomme afferenter (MIA) definert som afferenter som har svært høye mekaniske terskler eller reagerer ikke på mekaniske stimuli.
Nociceptorer kan klassifiseres etter ledningshastigheten til deres aksoner eller fiberdiameter, dette er henholdsvis gruppe III og IV ord Aδ og C.
Type Aδ myelinerte afferenter med middels diameter som formidler akutt, godt lokalisert, skarp stikkende smerte, kjent som gruppe III afferent. Aδ-afferente fibre har gjennomsnittlig fiberdiameter 2-5 mm og ledende hastighet 5-30 m / s. Aδ-nociceptorer kan deles inn i to typer (det ser ut til å eksistere omtrent 50% av hver type)
- Type I Aδ er mekanisk følsomme afferenter (MSA) som reagerer med en langsomt tilpasningsutslipp til sterk punkter punktet.De reagerer også på varme og kjemiske stimuli og har relativt høye varmeterskler (> 50C).
- Type II Aδ-nociceptorer har lavere varmeterskel enn Type I-enheter, men har svært høye mekaniske terskler (kalt mekanisk ufølsomme afferenter – MIA). Aktiviteten til denne afferente formidler nesten helt sikkert den «første» akutte smertesvaret mot skadelig varme. De er rapportert i kneleddet, innvollene og hornhinnen.
Type C umyeliniserte afferente fibre som formidler dårlig lokalisert kjedelig, svie, såkalt «andre» eller langsom smerte er kjent som gruppe IV. Gjennomsnittlig fiberdiameter er under 2 mm og ledende hastighet er 2 m / s eller mindre. De umyeliniserte C-fibrene er også heterogene. C-fiberafferenter kan deles i to klasser basert på deres respons på mekaniske stimuli. I likhet med de myeliniserte Aδ-afferente fibrene er de fleste C-fibre polymodale, det vil si at de inkluderer en populasjon som er både mekanisk og varmefølsom (CMH). Responsen fra CMH er også sterkt påvirket av stimulushistorien. Både tretthet og sensibilisering er observert. En reduksjon i responsen på varme observeres også etter mekaniske stimuli påført det reseptive feltet eller elektriske stimuli på nervestammen. Dette antyder at tretthet som respons på en gitt stimulusmodalitet kan induseres av heterolog stimulering, det vil si ved eksitasjon med en stimulus av en annen modalitet. Dette er den dominerende typen C-fiber nociceptorer i pattedyrs hud. Mekanisk ufølsomme C-fibre (C-MIAer) reagerer enten ikke på mekaniske stimuli eller har en veldig høy mekanisk terskel. Disse afferentene reagerer på varme og ulike skadelige kjemiske stimuli (f.eks. Capsaicin, histamin) og blir ofte ansett for å være kjemoreseptorer.
Oppsummert til det ovenstående er umiddelbar, godt lokalisert, gjerrig smertefølelse formidlet av myeliniserte nervefibre med liten diameter, type Aδ. C-fibre formidler dårlig lokalisert anatomisk smerte, den har vondt og brennende karakter, kommer senere enn den første sensasjonen, og det er vanskelig å estimere dens styrke.
TRP-kanaler
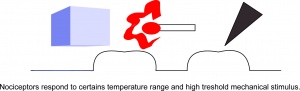
Nociceptorer reagerer på bestemt temperaturområde og mekanisk stimulans.
Den perifere enden av aksonen inneholder innkapslede proteiner kalt transduksjonsproteiner (TRP), som kan aktiveres av en spesifikk stimulans. Den transiente reseptorpotensialet (TRP) multigen-superfamilien koder for integrerte membranproteiner som fungerer som ionekanaler. TRP-kanalfamilien er av interesse fordi flere medlemmer har blitt involvert i transduksjon av nociceptorsignaler.
Skadelig kulde og skadelig varmestimuli oppdages av Aδ- og C-fibernociceptorer. TRP-kanalfamilien gir en gruppe molekyler utstyrt for å oppdage termiske endringer. Hele temperaturområdet, fra skadelig kulde til skadelig varme, ser ut til å bli transdusert av aktiviteten i disse ionekanalene. TRPM8 og TRPV3 / 4 koder henholdsvis kjølig og varm, TRPA1 overfører skadelig kulde og TRPV1 / 2 fornemmer skadelig varme. Noen av de termosensitive TRP-kanalene reagerer også på kjemiske og mekaniske stimuli.
For eksempel er TRPV1 viktig for å transdusere nociceptiva ved inflammatoriske og hypotermiske effekter av vanilloidforbindelser og bidrar til akutt termisk nociception og termisk hyperalgesi etter vevskade. TRPV1-strøm forsterkes av bradykinin og nervevekstfaktor via flere mulige mekanismer og aktiveres også av protoner og capsaicin, den ‘‘ varme ’’ forbindelsen i chilipepper. I motsetning til hyperalgesi etter intense skadelige stimuli, kan langvarig eksponering for capsaicin resultere i påfølgende desensibilisering.
Mens oppdagelsen av termosensitive TRP-kanaler i stor grad har forbedret vår forståelse av transduksjonsmekanismer for termiske stimuli, er funn hos dyr med selektive gendelesjoner tydelig. indikerer at flere og ennå ukjente transduksjonsmekanismer er engasjert av termiske stimuli.
Kjemiske meglere
Skader resulterer i lokal frigjøring av mange kjemikalier fra ikke-neuronale celler (f.eks. fibroblaster, mastceller, nøytrofiler, monocytter og blodplater), samt fra sensoriske terminaler til primære afferente fibre som formidler eller letter betennelsesprosessen. Inflammatoriske mediatorer inkluderer prostaglandiner, leukotriener, bradykinin, serotonin, histamin, SP, tromboksaner, blodplateaktiverende faktor, puriner som adenosin og ATP, protoner og frie radikaler. Cytokiner, slik som interleukiner og tumornekrosefaktor, og nevrotrofiner, spesielt NGF, genereres også under betennelse.Det er verdt å merke seg at de fleste av disse kjemikaliene (hovedsakelig stoffer som bradykinin og prostaglandin E2) generelt anses å ikke aktivere nociceptorer direkte, men heller forsterker følelsen av smerte som respons på naturlige stimuli og andre endogene kjemikalier ved å øke handlingsfrekvensen. potensiell avfyring.
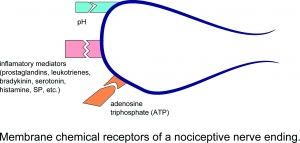
Membrankjemiske reseptorer for en nociceptiv nerveende.
Aktivering av nociceptorer overfører ikke bare afferente meldinger til ryggmargs dorsale horn, men initierer også prosessen med neurogen betennelse. Nevrogen betennelse forårsaker frigjøring av nevrotransmittere, særlig substans P og kalsitoningener-relatert peptid (CGRP), som fører til alvorlig vasodilatasjon, samt plasmalekkasje av proteiner og væske fra post kapillære vener.
To kjemikalier er av spesiell interesse:
- Adenosintrifosfat (ATP)
ATP er det energibærende molekylet i alle kroppens celler. Det frigjøres fra alle vev under traumer og andre patologiske endringer som er forbundet med celledød. Av denne grunn har ATP blitt ansett som et generelt signalstoff for vevstraumer og smerter. I humane mikronurografiske studier aktiverte injeksjon av ATP 60% av mechano-responsive og mechano-følsomme C-nociceptive fibre uten å sensibilisere disse fibrene for mekaniske eller varme stimuli. ATP aktiverer purinergiske P2X3-reseptorer i nociceptorer som forårsaker utslipp. ATP er spesielt viktig for muskelsmerter fordi det er tilstede i muskelceller i høy konsentrasjon.
- Protonerendring i vevets pH
Syrefølende ionekanaler (ASIC) utgjør en familie av reseptormolekyler som er følsomme for et fall i pH og åpne ved forskjellige pH-verdier. Kanalproteinene reagerer allerede for små pH-endringer. Denne reseptorfamilien (for eksempel ASIC1 og ASIC3) er spesielt viktig for muskelsmerter fordi nesten alle patologiske forandringer i muskler er ledsaget av et fall i vevets pH, f.eks. Utmattende trening, iskemi og amming.
Nociceptors plassering
Nociceptors cellelegemer er lokalisert i dorsalrotganglier (DRG) for periferien og trigeminusganglier for ansiktet. Axonene deres strekker seg inn i det perifere nervesystemet og slutter i grener som skaper mottakelige felt.
- Hud
Frie nerveender som slutter i huden er maskineriet for å signalisere lokale mekaniske, termiske og kjemiske endringer. Det store flertallet av frie nerveender i huden kalles polymodale nociceptorer fordi de inneholder flere reseptorer og dermed reagerer på forskjellige kombinasjoner av ovennevnte stimulus. Type I Aδ-høyterskelmekanoreceptorenheter er tett fordelt i hårete og glatt hud.
- Muskler
Reseptormolekyler som er spesielt viktige for funksjon av muskelnociceptorer er syrefølende ionekanaler (ASIC) som åpnes ved lavt vevs pH, P2X3-reseptorer som aktiveres ved binding av adenosintrifosfat (ATP), og den forbigående reseptorpotensialreseptorundertype 1 (TRPV1) som er følsom for høy temperaturer og lav pH.
I skjelettmuskulatur ser de frie nerveendene ut til å være fordelt ganske jevnt. Det ble ikke funnet noen forskjell mellom de proksimale og distale delene av rotte gastrocnemius – soleus muskel. I den samme studien ble det imidlertid funnet at nervefibretettheten i peritendineum av rottekalkaneal sene var flere ganger høyere enn i GS-muskelen. I motsetning til dette var kollagenfibrene i selve senevævet nesten fri for frie nerveender.
- Sener
Innervasjon av akillessener menneskelig leveres av nerver fra de omkringliggende musklene og av små fasciculi fra kutane nerver, men dette involverer all nerveenden. Gratis nerveender er representert inne i senene, men hovedsakelig i peritendinøst vev, er smertereseptorer. Antall og plassering av alle nervefibre og nerveender varierer avhengig av senefunksjonen, og er mer representert i de mindre senene som er involvert i fine bevegelser.
- Ledd
Nociceptorer i leddene er plassert i leddkapsel, leddbånd og proksimale sener, bein, periosteum, leddfettpute og rundt blodkar, men ikke i leddbrusk. Høytterskel nociceptive afferenter slutter primært i synovium og periosteum og reagerer normalt bare på bevegelsen av leddet utover arbeidsgrensene. Etter leddskade kombineres to faktorer for å endre den mekaniske følsomheten til leddnociceptorer.For det første endrer fysiske endringer (leddeffusjon og vevsødem) de hvilende og bevegelsesinduserte kreftene som utøves på leddvevet, og for det andre, sensibiliserende mediatorer som frigjøres i det skadede vevet, sensibiliserer artikulære nociceptive afferenter ved å binde til reseptorer på nerveender. Mange nociceptorer i leddet reagerer på uskadelige bevegelser, men aktiveres i økende grad når bevegelser overskrider det fysiologiske arbeidsområdet, mens andre nociceptorer bare er aktive under skadelige bevegelser. Den tredje gruppen av såkalte lydløse nociceptorer er normalt inaktive og reagerer bare under patologiske omstendigheter, som for eksempel ved amming.
Det er vist at korselen i korsryggen er rik innerveret av nociceptorer og proprioceptive fibre. I normal tilstand har nociceptorer som de som er sett i fasettleddkapslen en høy terskel og forventes ikke å slippe ut med mindre belastning er suprafysiologisk. Imidlertid, i nærvær av patologisk leddbetennelse, kan synovittkjemiske mediatorer sensibilisere disse nociceptorene, og suprafysiologiske nivåer av stress kan ikke lenger være nødvendig for å stimulere smerte. Slike inflammatoriske mediatorer (substans P, bradykinin, fosfolipase A2) er blitt påvist i fasettleddkapslen.
Nociceptorer i mellomvirvelskiver er normalt begrenset til den ytre tredjedelen av ringrommet, kan være substratet for diskogen smerte når de utvides over det større ringformede området og trenger lenger inn i den utartede skiven langs vaskulaturen og fi surer. Disse C- og A δ-fibrene er sannsynligvis ansvarlige for å overføre smertesvar. Det bakre langsgående leddbåndet og de ytre ringformede fibrosuslagene på mellomvirvelskiven inneholder rikelig med nociceptive ildfibre. Nervefibre og nerveender forekommer også i det subkondrale beinet i de zygapofysiale leddene. De forekommer i erosjonskanaler som strekker seg fra det subchondrale beinet til leddbrusken.
En menneskelig studie av (Kiter et al., 2010) viste både frie og innkapslede nerveender i det humane iliolumbar ligamentet. Studie av (Hirsch et al., 1963) foreslo tilstedeværelsen av fin nervefibre og komplekse uinnkapslede ender i de supaspinøse og intraspinøse ledbåndene.
- Viscera
Viscerale nociceptorer reagerer ikke på kutte- eller brenneskader som deres kolleger i perifert kutanvev. I stedet aktiveres de som svar på patologisk endring. Smerteproduserende stimuli i innvollene, inkludert trekkraft på mesenteriet, betennelse, utspenning av hule muskelveggede organer som gastrointestinale, urinveier, galleblære og sterke sammentrekninger av muskellag som omgir slike hule organer, kjemikalier irriterende eller iskemi i organer som hjerte. Fordelingen av disse ildene varierer mellom organer. Høyterskelreseptorer utelukkende innerverte organer der smerter er den eneste bevisste følelsen (dvs. urinleder, nyre, lunger, hjerte), men er relativt få i organer som gir uskadelige og skadelige opplevelser (f.eks. Tykktarm, mage og blære), innerveres hovedsakelig av lavterskelreseptorer. Organer, som lever, lunger, nyrer og bukspyttkjertel, har få reseptorer, men smertene fra disse organene kommer hovedsakelig fra aktivering av reseptorer i kapslene i disse organene. Nociceptiv stimulering av innvoller fører til diffus smerte som er vanskelig å lokalisere. Afferente nociceptive fibre i innvoller er funnet i forbindelse med sympatiske og parasympatiske nerver. Flertallet av viscerale organer er innerveret av vagal nerve, men studier viser ikke klart om denne nerven er i stand til å bære nociceptive afferent input. Imidlertid viser noen studier tydelig at vagale afferenter formidler informasjon om mekaniske stimuli med høy intensitet til sentralnervesystemet. En rekke studier som involverer mennesker eller dyr har vist at forsøkspersoner med spinal cor lesjon er i stand til å rapportere smerter som sannsynligvis stammer fra området med innvollsorganer.
- 1.0 1.1 Loeser JD, Treede RD. Kyoto-protokollen til IASP Basic Pain Terminology. Smerte. 2008; 137 (3): 473–7. doi: 10.1016 / j.pain.2008.04.025. PMID 18583048
- Basbaum AI, Jessell T. The Perception of Pain. I: Kandel ER, Schwartz J, Jessell T. redaktører. Prinsipper for nevrovitenskap. New York: Appleton og Lange; 2000. p472-491
- 3.0 3.1 3.2 3.3 3.4 3.5 Meyer RA, Ringkamp M, Campbell JN, Raja SN. Perifere mekanismer for kutan nociception. I: McMahon SB, Koltzenburg M, redaktører. Wall and Melzack’s Textbook of Pain. London: Elsevier; 2006. s3–34.
- Lloyd DPC. Nevronmønstre som styrer overføring av ipsilaterale bakre reflekser hos katt. J Neurophysiol. 1943; 6: 293–315
- 5.0 5.1 5.2 Schaible HG, Schmidt RF. Effekter av en eksperimentell leddgikt på de sensoriske egenskapene til fine artikulære afferente enheter. Journal of Neurophysiology. 1985; 54: 1109-1122
- Häbler HJ, Jänig W, Koltzenburg M.En ny type umyelinisert kjemosensitiv nociceptor i den akutt betente urinblæren. Agenter og handlinger. 1988; 25: 219-221
- Tanelian DL. Kolinerge aktivering av en populasjon av afferente nerver i hornhinnen. Eksperimentell hjerneforskning. 1991; 86: 414-420
- LaMotte RH, Campbell JN. Sammenligning av responser av varme og nociceptive C-fiber afferenter i ape med menneskelige vurderinger av termisk smerte. Journal of Neurophysiology. 1978; 41: 509-528
- Treede RD, Meyer RA, Raja SN, Campbell JN. Bevis for to forskjellige varmetransduksjonsmekanismer i nociceptive primære afferenter som innerverer apeskinn. Tidsskrift for fysiologi. 1995; 483: 747-758
- Schepers RJ, Ringkamp M. Thermoreceptors and thermosensitive afferents. Nevrovitenskap & Bioadferdsmessige anmeldelser. 2010; 34 (2): 177-184
- Caterina MJ, Schumacher MA, Tominaga M, Rosen TA, Levine JD, Julius D. Capsaicinreseptoren: en varmeaktiverte ionekanal i smerteveien. Natur 1997; 389: 816–824
- Bjur D, Alfredson H, Forsgren S. Innerveringsmønsteret til den menneskelige akillessenen: studier av den normale og tendinose-senen med markører for generell og sensorisk innervering. Cell Tissue Res. 2005; 320: 201-206
- 13.0 13.1 Ashton IK, Ashton BA, Gibson SJ, Polak JM, Jaffray DC, Eisenstein SM. Morfologisk grunnlag for ryggsmerter: demonstrasjon av nervefibre og nevropeptider i korsryggen i korsryggen, men ikke i ligamentum fl avum. J Orthop Res. 1992; 10 (1): 72-78
- Kiter E, Karaboyun T, Tufan AC, Acar K. ImmunohistochemicalfckLRdemonstrasjon av frie nerveender i iliolumbar ligament. Ryggrad. 2010; 35 (4): E101-4. doi: 10.1097 / BRS.0b013e3181ae561d.
- Hirsch C, Ingelmark BE, Miller M. Det anatomiske grunnlaget for lowfckLRback smerter. Studier på tilstedeværelsen av sensoriske nerveender infckLRligamentøse, kapsulære og intervertebrale skivestrukturer i fckLRhuman lumbal ryggrad. Acta Orthop Scand. 1963; 33: 1–17.
- Moller, Aage (2014-04-22). Smerter, dens anatomi, fysiologi og behandling. Kindle Edition.
