学習目標
- 書く酸および塩基として作用する水の化学方程式。
水(H2O)は、多くの点で興味深い化合物です。ここでは、酸または塩基として機能する能力について検討します。
状況によっては、水分子がプロトンを受け入れ、ブレンステッド-ローリー塩基として機能します。 HClをH2Oに溶解する例を見ました:
\
他の状況では、水分子がプロトンを供与して、ブレンステッド-ローリー酸として機能することがあります。たとえば、アミドイオンの存在下(セクション10.2の例4を参照)では、水分子がプロトンを供与し、生成物としてアンモニアを生成します。
\
この場合、 、NH2-はブレンステッド-ローリー塩基(プロトンアクセプター)です。
したがって、状況に応じて、H2Oはブレンステッド-ローリー酸またはブレンステッド-ローリー塩基のいずれかとして機能します。水は、酸として反応する場合もあれば塩基として反応する場合もある唯一の物質ではありませんが、確かに最も一般的な例であり、最も重要な例です。状況に応じてプロトンを供与または受容できる物質は、両親媒性化合物と呼ばれます。
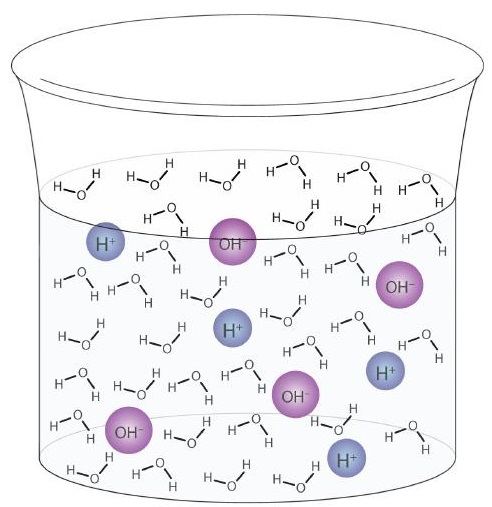
水分子は、純水のサンプルでも酸または塩基として機能します。 1億個に6個(108個に6個)の水分子が次の反応を起こします。
\
このプロセスは水の自動イオン化と呼ばれます(図\(\ PageIndex {1} \))純粋であるか溶液の一部であるかにかかわらず、水のすべてのサンプルで発生します。自動イオン化は、両親媒性液体である程度発生します。 (比較のために、液体アンモニアも自動イオン化を受けますが、10億分の1(1015分の1)だけが別のアンモニア分子と反応します。)
コンセプトレビュー演習
- 水が酸としてどのように機能するかを説明します。
- 水が塩基としてどのように機能するかを説明します。
回答
- 適切な条件下で、H2Oはプロトンを供与して、ブレンステッド-ローリー酸にします。
- 適切な条件下で、H2Oはプロトンを受け入れ、ブレンステッド-ローリーにします。塩基。
重要なポイント
- 水分子は、場合によっては酸と塩基の両方として機能します。条件。
