症例:高血圧、冠状動脈疾患、および以前の心筋の病歴を持つ73歳の男性梗塞(MI)は、疲労、息切れ、尿量の減少、足首の腫れを伴って救急科(ED)に現れます。到着時の彼のバイタルサインには、BP 87/58 mm Hg、HR 102、RR 24、室内空気でのT飽和度86%、温度98.2 Fが含まれ、聴診でパチパチ音がします。この患者をどのように管理しますか?
心原性ショックとは何ですか?
定義はさまざまですが、心原性ショック(CS)は、関連する心原性ショックの状態として広く定義されている臨床診断です。不十分な末端器官灌流、または心臓損傷に続発する組織低灌流。 1 SHOCK試験から導き出された一般的に使用される基準は、低血圧(SBP < 90mmHgまたは> 90mmHgと支持療法)、終了の証拠臓器低灌流、および心係数(CI)< 2.2 L / min / m2または肺動脈楔入圧≥15mmHg2,3この定義は、臨床試験の選択基準を標準化するのに役立ちますが、救急科(ED)でCSを診断することはあまり価値がありません。忙しいEDのシフトでは、CSは、多様な症状、他のショック状態(すなわち敗血症)との重複、よく理解されていない病態生理学、複雑で多因子的な原因、およびさまざまな血行力学的パラメーターのために診断が難しい場合があります4。侵襲性心拍出量がない場合(CO)およびPCWP値、CSは、充満圧の上昇(すなわち、肺うっ血またはJVPの上昇)の証拠、低灌流の臨床的兆候、および心不全を示唆する病歴およびエコーを使用して推測できます。 CSに続発する死亡率は高い(〜25-70%)が、早期の認識と介入により生存率が向上する4,5。救急医は入院時にCSを診断する機会があり、重症患者を診察する際には高い臨床的疑いを維持する必要がある。このレビューでは、身体検査、ラボ、ベッドサイドの超音波検査、および画像診断を通じてCSの診断を見逃さないための認識とヒントに焦点を当てます。
心原性ショックの原因は何ですか?
CSのほとんどの研究は、左心室が関与する心筋梗塞(MI)に続発するCSの患者に焦点を合わせています。 MIはCSの主な原因(〜70%)ですが、心室機能障害の原因、および潜在的な原因としてCOまたは心係数(CO /体表面積)の低下を考慮する必要があります6。これには、以下が含まれますが、これらに限定されません。右心不全、心筋炎、たこつぼ型心筋症、肥大型心筋症、または心臓弁膜症の非虚血性の原因(表1)。物事をより困難にするために、CSは、心不全の悪化から不可逆的な末端器官損傷を伴う難治性ショックに至るまで、静的な状態ではなく連続体です(図1)。 CSは、不整脈や進行性虚血およびアシドーシスなどの二次的発作の発生によりさらに変動しやすくなります。3症例の2/3では、CSは入院時に存在せず、その後、患者として入院してから48時間以内に発症することに注意してください。ショックの連続体を進行します。7患者の生命徴候、症状、身体検査、およびベッドサイドエコーを頻繁に再評価することが重要です。

表1:Parrillo & Dellinger(2013)から採用されたCSの原因8 CS症例の70%は急性MIが原因です。6関連する急性MIの影響SHOCKトライアルレジストリの結果から得られたパーセンテージ。9.10
図1:Bellumkonda etalから適合したCSの連続体。 (2018).3このスペクトルは、二次的発作(例:新しい不整脈)によって逸脱する可能性があります。
心原性ショックの死亡率
CSに続発する死亡率は高いままですが、4早期の認識と介入SHOCK試験登録を含むデータを使用すると、急性MIによる左心室(LV)または右心室(RV)の障害に続発するCSと診断された1,217人の患者の30日間の院内死亡率は57%でした。 。いくつかの危険因子、特に入院時のショック、年齢、以前の冠状動脈バイパス移植(CABG)、非劣性MI、クレアチニン> 1.9 mg / dL、SBPの低下、無酸素脳損傷、および末端器官の低灌流の臨床的証拠により、患者は12%から88%の範囲の死亡率で細分化される可能性があります11。GRACE試験では、CSは1999年から2006年の間に弱く、しかし有意に減少しました。冠状動脈インターベンション(PCI)、CSを合併したMI患者の早期介入の重要な形態12。危険因子に基づいて患者を層別化する場合でも、PCIとCABGは低リスク患者と高リスク患者の両方に利益をもたらしました。11早期診断と適切な治療が残っており、特に心筋虚血の場合、CS患者の転帰の重要な修正可能な要因です。
さらに、CSの進行が長ければ長いほど、不適応な炎症が起こる可能性が高くなります。心臓の活動を阻害するTNF-αやIL-6などのサイトカインの増加に続発する反応。 4,13バソプレッシンとアンジオテンシンIIの増加もあり、これは後負荷を増加させ、COを悪化させ、水分と塩分の保持を増加させ、それによって肺水腫を引き起こします。一酸化窒素(NO)も、NOシンターゼの活性化によって増加し、血管拡張と心筋の鬱病を引き起こします。低COおよび心筋虚血に対するこれらすべての不適応反応は、心臓組織の損傷の悪化、COの低下、および分布性ショックにつながります。心不全の危機に瀕している患者が積極的な利尿薬、硝酸塩、ベータ遮断薬、ACEI、およびモルヒネで治療される場合、CSのいくつかの症例は医原性であることに注意する必要があります。 14したがって、患者を評価する最初の医師として、救急医は時間に敏感で臨床的に適切な方法でCSを特定して治療する必要があります。
臨床評価
通常、CSの患者呼吸困難、胸痛、疲労、および/または足首の腫れを訴えます。灌流が不十分な四肢(表2)。未分化ショックの30人の患者の小規模な回顧的レビューでは、CSの患者はJVD(0%および20%と比較して80%)、冷えた皮膚(14.3%および.28.5%と比較して57.1%)、および肺を有する可能性が高かった分布性ショックおよび血液量減少性ショックの患者と比較して、それぞれラレス(75%対16.7%および8.3%)16。68人の患者を対象とした別の前向き研究では、居住者は特定の臨床検査所見を使用してショックのカテゴリーを区別しました。 CSは、SBPが90未満、低出力の兆候(冷たい手、毛細血管の補充不良、脈拍の弱さ)、頸静脈圧(JVP)の上昇によって分類されました> 7 cmH2O、S3ギャロップ、および肺の3分の1にパチパチ音をたてる。 68人の患者のうち、11人がCSの基準を満たしました。心拍出量が低いという心エコー検査の証拠がある患者では、JVPの上昇によりCSが80%の精度で予測されましたが、クラックルの存在を追加しても変化しませんでした。17
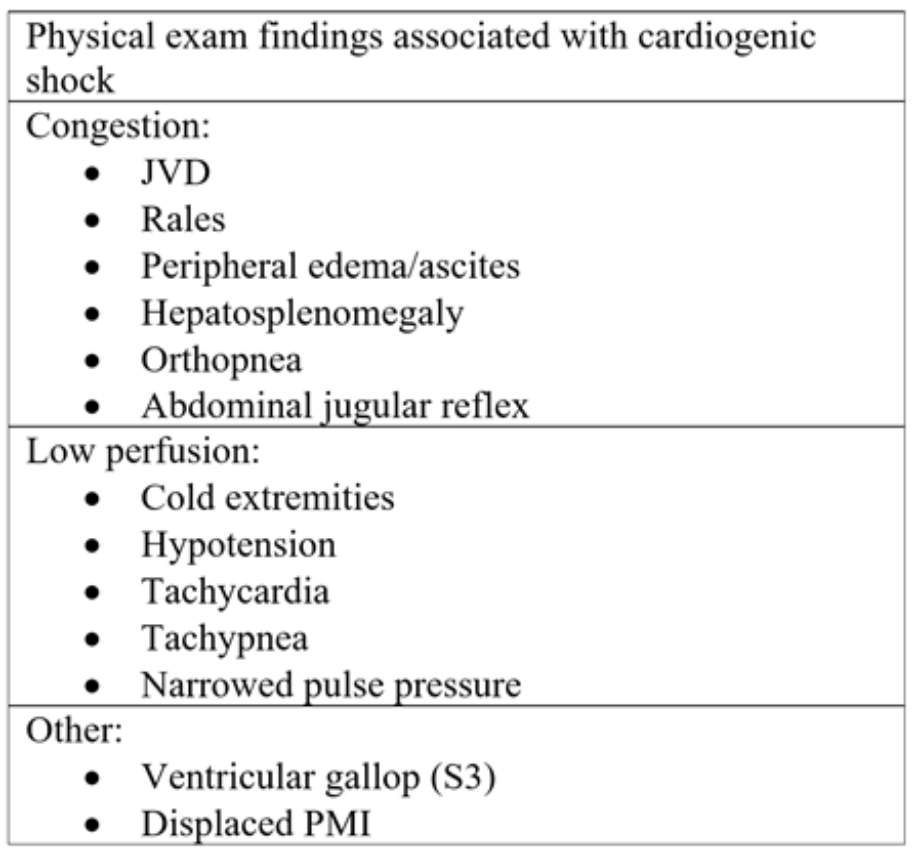
表2:急性心不全とその後の心拍出量ショックで見られる身体検査の要素18
JVPはウェッジ圧の上昇の有用な代用物ですが19、評価が難しい場合があります体の習慣と患者の体位により(ベッドの頭は45度高くする必要があり、重度のオルソプネアの患者では困難な場合があります)20 JVPは、胸骨角より上のcm単位の最高脈動点を計算して5を加算することによって測定されます。 (右心房は胸骨角より5 cm下にあるため)、これはcmH20の膨張と相関します(図2)。値の上昇は、6〜8 cmH20.18より大きいと見なされることがよくあります。注目すべきことに、JVPの上昇は、死亡リスクの増加と関連しており、相対リスク(RR)は1.52.18
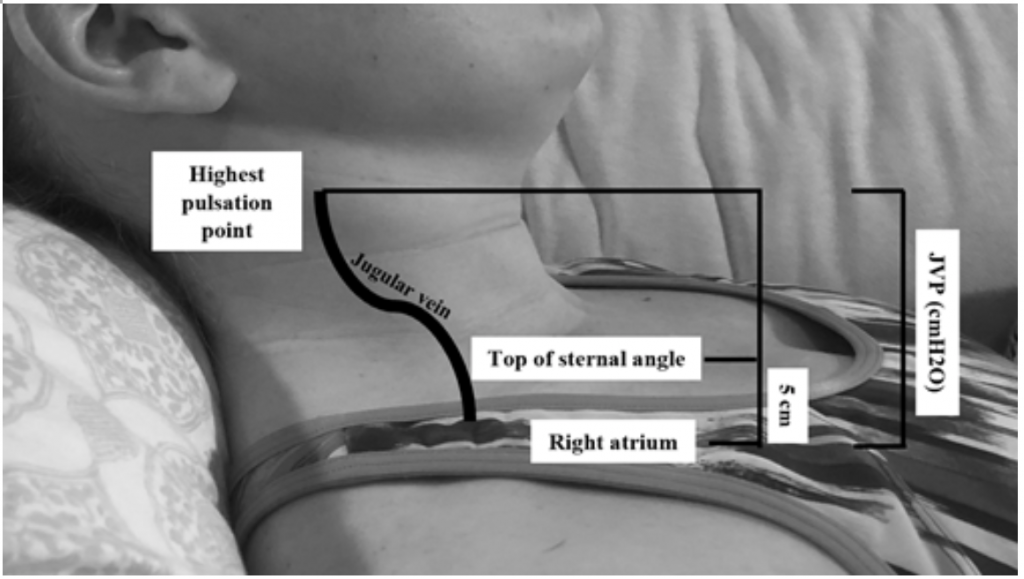
図2:Shah & Cowger(2014).18
ラボから採用されたJVPの測定代謝性アシドーシス(末梢虚血により乳酸塩が増加するため)、急性腎障害を伴う腎低灌流、およびトロポニンとEKGの変化の上昇を伴う心臓虚血の可能性のある証拠15。CardShock研究では、219CSの多施設前向き観察研究患者の場合、乳酸塩レベルは死亡率の増加と有意に関連していました(調整オッズ比1.4)6。乳酸塩の上昇は敗血症に固有のものではなく、CSなどの低灌流状態で見られることに注意することが重要です。
一方、これらの身体検査の所見と血行力学的パラメーターは常に当てはまるとは限りません。 SHOCK Trialレジストリを使用した研究では、CS患者の5.2%は、末梢低灌流と低CIの兆候があったものの、明白な低血圧はありませんでした21。 SVR)であり、一時的に血圧を維持しますが、一般的に脈圧は狭くなります22。イメージングで臨床的に重大な肺水腫を患っている患者でさえ、うねりではなく、喘鳴または明確な肺音を示すことがあります23。ある研究では、肺うっ血はMIに続発するCSの約2/3例。21さらに、LV収縮性が低下したとしても、CS患者はLVEFの深刻な低下を示さない可能性があります。 14,24実際、CS患者のコホートの平均EFは約30%であり、これは減少していますが、予想よりも高くなっています。2
試験は完璧ではありませんが、バイタルサインと検査室の注意深いレビューとともに、うっ血と末梢低灌流の兆候を探す詳細な身体検査が、患者が心原性ショックを患っている最初のヒントになる場合があります。
心原性ショックを評価するためのポイントオブケアECHO
患者が低血圧または低灌流のEDに来院した場合、RUSH検査は、「ポンプ」を調べることでショックを区別する簡単な方法です。 25,26 CSの場合、経胸壁心エコー図は、古典的に、収縮期および拡張期のLV圧迫が不十分で、僧帽弁の前尖の動きが不十分である(すなわち収縮性が低い)低血圧の拡張LVを示します。単純な「眼球運動」LV圧迫による排出率(EF)およびCO(CO =脳卒中量(SV)x心拍数(HR)として)の推定は、急性期の医師による適切な評価です。27CSでは、下静脈効果的なイントラの間接測定であるcava(IVC)血管容積は、直径> 2 cmで、インスピレーションによって50%未満崩壊する必要があります。これらの所見は中心静脈圧の上昇と相関しています28。ただし、患者がすでに血管拡張薬、利尿薬を投与されている場合、および/または換気されている場合は、IVC評価が不正確になる可能性があります29。胸窓は過剰なBの形で肺水腫を示す可能性があります間質内の水分蓄積による中隔肥厚の結果である線(「肺ロケット」)。30肺うっ血に加えて、RUSH検査では胸水および腹水が存在する可能性があります。253つの元のデータを使用したメタアナリシスでは論文と2つの症例報告では、RUSHプロトコルはCSの診断において感度と特異性の両方(それぞれ0.89と0.97)であることが示されました31。22.29の高い結果の陽性尤度比(LR)にもかかわらず、中程度の陰性しかありませんでしたLRが0.17であり、RUSH検査はCSを除外するための完全な検査ではないことを示唆しています。したがって、RUSH検査は、心原性を診断するために単独で使用するのではなく、注意深い病歴および身体検査の文脈で使用する必要があります。 cショック。
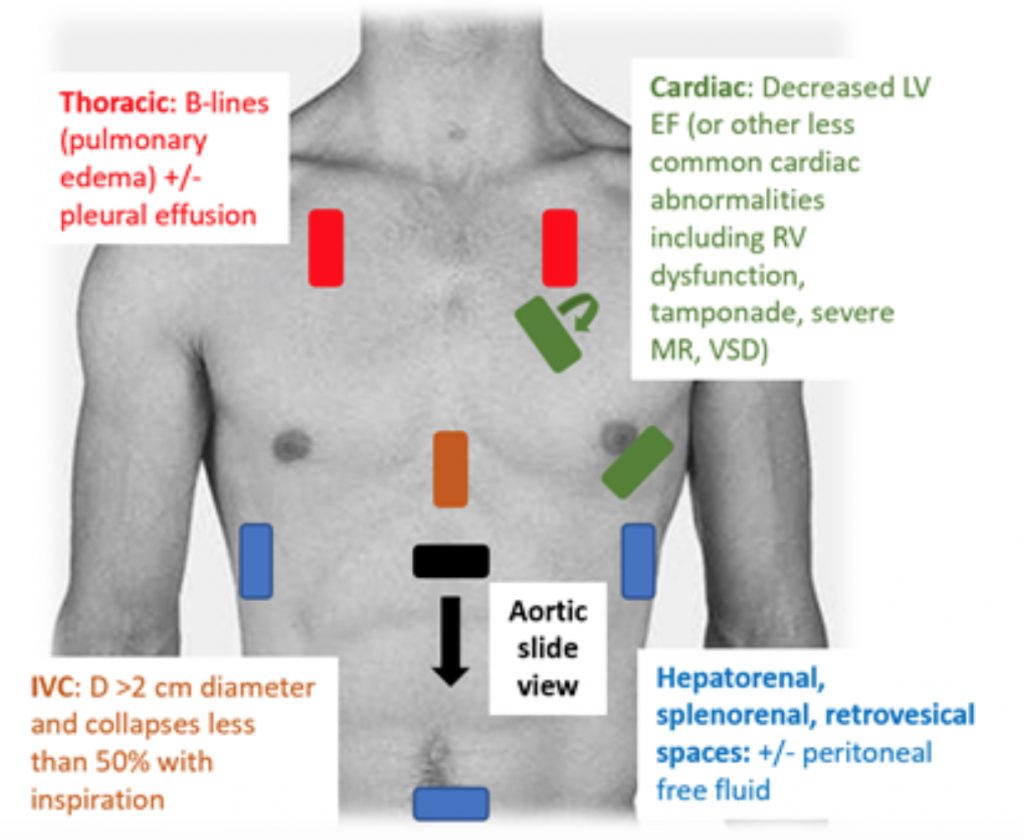
図3:未分化低血圧の評価のためのRUSHベッドサイド米国試験とCS.25を示唆する関連所見、26,29,30
「眼球運動」によってCOを推定するだけでなく、超音波でCOを測定する1つの方法は、最初に左心室流出路速度時間間隔(LVOT VTI、または速度)を使用してSVを決定することです。大動脈流出路での血流量)とLVOT径。具体的には、SV、つまり1拍あたりの左心室から排出される血液の量は、LVOT VTI×LVOTの断面積によって計算されます。32LVOTの直径を測定するには、フェーズドアレイプローブを胸骨傍の長軸ビューに配置し、収縮中期の大動脈弁のすぐ上のLVOTの距離。 VTIは、心尖部5腔像で測定されます。パルス波ドップラーモードを使用して、ドップラー波が大動脈弁のすぐ上に配置され、ドップラー波形が記録されます。過大/過小評価を避けるために、軸を可能な限り流出路に合わせるようにしてください。 「LVOTVTI」測定ツールを選択した後、1回の駆出周期の波形を測定します。33,34通常のLVOT VTIの範囲は18〜22 cmですが、HR > 95bpmでは低くなる可能性があります。 35心房細動の患者では、VTI測定値が真の値を過小評価する可能性が高いため、3〜5回の連続波形を平均化することをお勧めします。予想どおり、低LVOTVTIと有害転帰の間には相関関係があります。32
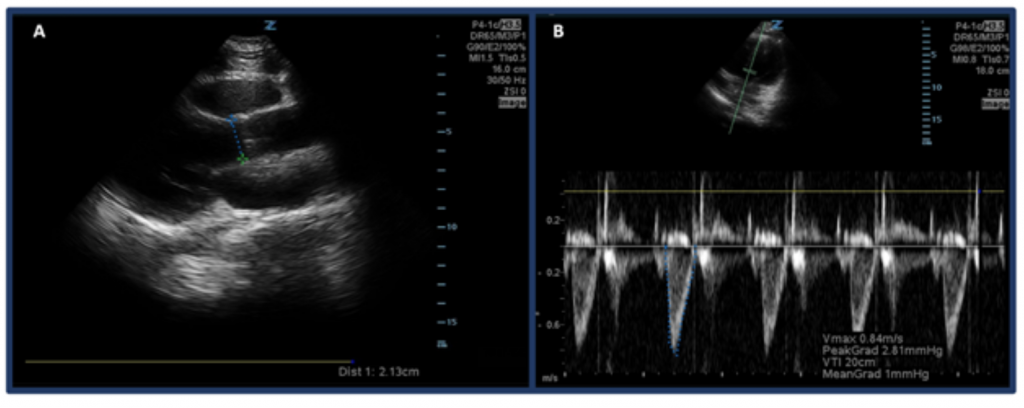
推奨される評価経路
上記のように、診断できる単一の検査結果やラボテストはありません。 CS。したがって、低血圧または低灌流の兆候の設定でCSの疑いが高い場合は、履歴、詳細な身体検査、ベッドサイドの米国、ラボ(特にクレアチニン、乳酸塩、トロポニン、BNPおよびその他の低灌流マーカー)を使用することをお勧めします/ end-organ-damage)、およびEKG(急性MIはCSおよび虚血の兆候の主な原因であり、緊急を必要とする場合があるため)血行再建術)診断を支援します(図5を参照)。 BPへの動脈カテーテルモニターを検討し、治療をガイドします。焦点を絞った心臓および肺の検査に加えて、身体検査はJVDおよび四肢灌流に焦点を合わせる必要があります。 RUSH試験と、上記のLVOTVTI測定によるEF / CO / CIの計算は、評価の貴重な補助手段です。包括的なアプローチを使用してCSを評価すると、この不均一な疾患をよりよく理解し、管理をガイドするのに役立ちます。
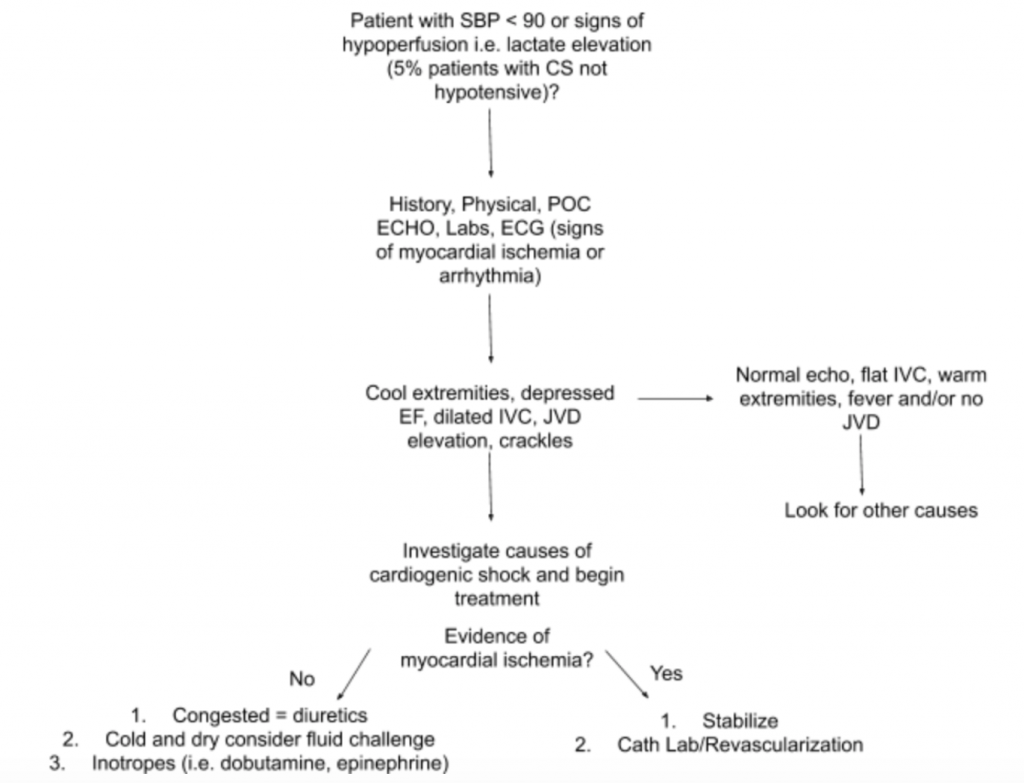
ケースの結論:さらに評価すると、患者の頸静脈圧は10 cmH20に上昇し、毛細血管の補充が遅れて足が冷えています。ベッドサイドのRUSH検査では、両側性のびまん性肺水腫と推定低EFが示されます。LVOTVTIはわずか10cmで測定されます。 EKGは、前頭葉リードのST上昇を示します。乳酸とトロポニンは穏やかに上昇しています。患者は、ドブタミン、IVフロセミド、およびCPAPの短期間の試験で安定し、バイタルサインと呼吸状態が中程度に改善された後、緊急PCIのためにカテーテル検査室に送られます。
持ち帰りポイント:
- CSは主に急性MI(〜70%)によって引き起こされ、ほとんどの研究の焦点ですが、他の原因も考慮する必要があります(を参照)。図1の完全なリスト)。
- CSに続発する死亡率は高いままです(〜60%)が、早期の特定と介入により生存率が向上します。
- 低灌流を探して注意深い身体検査を行い、混雑。 JVPは、CSの診断のための重要な身体検査コンポーネントであり、死亡率の増加に関連しています(RR = 1.52)。
- RUSH検査は、診断において感度が高く、特異的です(それぞれ、0.89と0.97)。 CS。ほとんどの患者は最初はCSに存在しないため、ベッドサイド超音波を頻繁に繰り返す必要があります。
- LVOT VTIの使用は、有害な結果に関連する測定値が低いCOを評価するためのシンプルで非侵襲的な方法です。
- 不均一な病状と症状に焦点を当ててCSが疑われる患者を評価するための推奨アプローチを図5に要約します。
FOAMed Resources:
- EM in 5 :ショック
- emDocs:心原性ショック
- emDocs:心不全のED管理-真珠と落とし穴
- emDocs:RUSH(「ショックのための迅速な超音波」)プロトコル
- emDocs:低血圧ED患者:順次体系的アプローチ
- 最初の10EM:未分化低血圧
