Tapaus: 73-vuotias mies, jolla on ollut verenpainetauti, sepelvaltimotauti ja aiemmin sydänlihas infarkti (MI) ilmaisee hätäosastolle väsymystä, hengenahdistusta, vähentynyttä virtsaneritystä ja nilkan turvotusta. Saapuessaan hänen elintoimintoihinsa kuuluvat verenpaine 87/58 mm Hg, HR 102, RR 24, T-kyllästys 86% huoneen ilmassa ja lämpötila 98,2 F, ja hänellä on rätinä auskultoinnissa. Kuinka hallitsisit tätä potilasta?
Mikä on kardiogeeninen sokki?
Vaikka määritelmät vaihtelevat, kardiogeeninen sokki (CS) on kliininen diagnoosi, joka on yleisesti määritelty alhaisena sydämen tehona ja siihen liittyvänä riittämätön elinelinten perfuusio tai kudoshypoperfuusio, joka johtuu sydänvaurioista. 1 Yleisesti käytetyt SHOCK-kokeesta saadut kriteerit koostuvat hypotensiona (SBP < 90mmHg tai > 90mmHg tukihoidolla), todisteista loppuhäiriöistä elimen hypoperfuusio ja sydänindeksi (CI) < 2,2 l / min / m2 tai keuhkojen kapillaarikiilapaine ≥ 15 mmHg 2,3 Vaikka tämä määritelmä on hyödyllinen kliinisten tutkimusten sisällyttämiskriteerien yhdenmukaistamiseksi , se on vähemmän arvokas CS: n diagnosoimiseksi hätäosastolla. Vaihdettaessa kiireisessä ED: ssä CS voi olla haastavaa diagnosoida monipuolisten esitysten, päällekkäisyyksien muiden sokkitilojen (eli sepsiksen), huonosti ymmärretyn patofysiologian, monimutkaisten ja monitekijöiden syiden ja vaihtelevien hemodynaamisten parametrien vuoksi. (CO) ja PCWP-arvot, CS voidaan päätellä käyttämällä todisteita kohonneista täyttöpaineista (ts. Keuhkojen ruuhkautuminen tai kohonnut JVP), hypoperfuusion kliinisistä oireista ja sydämen vajaatoimintaan viittaavasta historiasta ja kaikusta. CS: n toissijainen kuolleisuus on korkea (~ 25-70%), mutta varhainen tunnistaminen ja puuttuminen parantavat selviytymistä. 4,5 Hätälääkäreillä on mahdollisuus diagnosoida CS, kun heidät otetaan vastaan, ja heidän on ylläpidettävä suurta kliinistä epäilyä nähdessään kriittisesti sairaita potilaita. Tässä katsauksessa keskitytään tunnistamiseen ja vinkkeihin siitä, miten CS-diagnoosia ei kannata hukata fyysisen kokeen, laboratorioiden, sängyn ultraäänen ja kuvantamisen avulla.
Mitkä ovat kardiogeenisen sokin syyt?
Suurin osa CS-tutkimuksista keskittyy potilaisiin, joilla on vasemman kammion sydäninfarktin (MI) aiheuttama toissijainen sydäninfarkti. Vaikka sydäninfarktit ovat sydäninfarktin ensisijainen syy (~ 70%), mahdollinen syy kammion toimintahäiriöön ja alentuneeseen CO- tai sydänindeksiin (CO / kehon pinta-ala) on otettava huomioon.6 Tähän sisältyy, mutta ei rajoittuen, oikean sydämen vajaatoiminnan, sydänlihastulehduksen, takotsubo-kardiomyopatian, hypertrofisen kardiomyopatian tai venttiilisen sydänsairauden ei-iskeemiset syyt (taulukko 1). Jotta asiat olisivat haastavampia, CS on jatkumo eikä staattinen tila, joka vaihtelee sydämen vajaatoiminnan pahenemisesta tulenkestävään sokkiin ja peruuttamattomiin loppuelinten vaurioihin (kuva 1). CS: stä tulee vieläkin vaihtelevampi toissijaisten loukkausten, kuten rytmihäiriöiden tai progressiivisen iskemian ja asidoosin, esiintyessä.3 On huomattava, että 2/3 tapauksista CS ei ole läsnä oton yhteydessä, mutta kehittyy myöhemmin 48 tunnin kuluessa sairaalahoidosta potilaana etenee sokin jatkuessa.7 On tärkeää arvioida usein uudelleen potilaiden elintoiminnot, oireet, fyysinen koe ja sängyn kaiku.

Taulukko 1: CS: n syyt, mukautettu Parrillo & Dellinger (2013) -ohjelmaan. 8 70% CS-tapauksista johtuu akuutista MI: stä. SHOCK-kokeilurekisterin tuloksista saadut prosenttiosuudet. 9.10
Kuva 1: CS: n jatko, mukautettu Bellumkonda et al. . (2018) .3 Tämä spektri voi poiketa toissijaisista loukkauksista (esim. Uudet rytmihäiriöt).
Kardiogeenisen sokin kuolleisuus
Vaikka sydänkohtaukseen liittyvä kuolevuus on edelleen korkea, 4 varhainen tunnistaminen ja puuttuminen parantamalla selviytymistä.5 SHOCK-tutkimusrekisteriä sisältävien tietojen perusteella 1217 potilaan 30 päivän sairaalakuolleisuus, jolla diagnosoitiin akuutin sydäninfarktin aiheuttama vasemman kammion (LV) tai oikean kammion (RV) toissijainen CS . Jos otat huomioon useita riskitekijöitä, erityisesti sokki valinnassa, ikä, edellinen sepelvaltimoiden ohitussiirto (CABG), huonompi sydäninfarkti, kreatiniini > 1,9 mg / dl, vähentynyt SBP, anoksinen aivovamma ja kliininen näyttö elinelinten hypoperfuusiosta, potilaat voidaan jakaa kuolleisuuteen 12%: sta 88%: iin. 11 GRACE-tutkimuksessa CS: t laskivat heikosti, mutta vähenivät merkittävästi vuosina 1999-2006, mikä johtui todennäköisesti perkutaanisten sepelvaltimointerventio (PCI), tärkeä varhaisen intervention muoto sydäninfarktista kärsiville potilaille, jotka komplisoituvat CS: n avulla.12 Vaikka potilaat ositettaisiin riskitekijöiden perusteella, PCI ja CABG hyödyttivät sekä matalan että korkean riskin potilaita.Varhainen diagnoosi ja asianmukainen hoito ovat edelleen etenkin sydänlihasiskemian yhteydessä, mikä on tärkeä muunneltava tekijä keuhkoahtaumatautipotilaiden tuloksiin. toissijainen vaste sytokiinien, kuten TNF-alfa ja IL-6, lisääntymiselle, jotka estävät sydämen aktiivisuutta. 4,13 Vasopressiinin ja angiotensiini II: n määrä on myös lisääntynyt, mikä lisää jälkikuormitusta, pahentaa CO: ta ja lisää veden ja suolan pidättymistä aiheuttaen siten keuhkopöhön. Typpioksidia (NO) lisätään myös NO-syntaasin aktivaation kautta, mikä johtaa vasodilaatioon ja sydänlihaksen masennukseen. Kaikki nämä huonosti sopeutuvat reaktiot matalaan CO- ja sydänlihasiskemiaan johtavat sydänkudosvaurioiden pahenemiseen, masentuneeseen CO: han ja jakautumishokkiin. On huomattava, että jotkut CS: n tapaukset ovat iatrogeenisiä, kun sydämen vajaatoiminnan partaalla olevia potilaita hoidetaan aggressiivisilla diureeteilla, nitraateilla, beetasalpaajilla, ACEI: llä ja morfiinilla. 14 Ensimmäisenä potilasta arvioivana lääkärinä ensiapulääkäreiden on siis tunnistettava ja hoidettava keuhkosyöpä aikaherkällä ja kliinisesti sopivalla tavalla.
Kliininen arviointi
Klassisesti potilaille, joilla on CS voi esiintyä hengenahdistusta, rintakipua, väsymystä ja / tai nilkan turvotusta.15 Fyysinen koe voi paljastaa ruuhkautumisen merkkejä, mukaan lukien perifeerinen ödeema, kaulalaskimon paisuminen (JVD), halkeamia / kohinoita auskultoinnissa ja hypoperfuusion merkkejä, kuten viileä, huonosti perfusoidut raajat (taulukko 2). Pienessä retrospektiivisessä katsauksessa, joka sisälsi 30 erilaistumattomassa sokissa olevaa potilasta, CS-potilailla oli todennäköisemmin JVD (80% verrattuna 0% ja 20%), kylmä iho (57,1% verrattuna 14,3% ja 28,5%) ja keuhkojen asteikot (75% vs. 16,7% ja 8,3%) verrattuna potilaisiin, joilla oli jakautuva ja hypovoleminen sokki.16 Toisessa prospektiivisessa tutkimuksessa, johon osallistui 68 potilasta, asukkaat käyttivät erityisiä kliinisen kokeen tuloksia erottamaan sokkiryhmät. CS luokiteltiin SBP: n mukaan alle 90, alhaisen tuotoksen merkit (kylmät kädet, huono kapillaarien täyttö ja heikko pulssi), kohonnut kaulalaskimon paine (JVP) > 7 cmH2O, S3 laukka ja repisee 1/3 keuhkoista. 68 potilaasta 11 täytti CS: n kriteerit. Potilailla, joilla on sydämen ultraäänitutkimuksia, joiden sydämen teho on alhainen, kohonnut JVP ennusti CS: n 80%: n tarkkuudella, joka ei muuttunut, kun lisättiin särkymiä.17
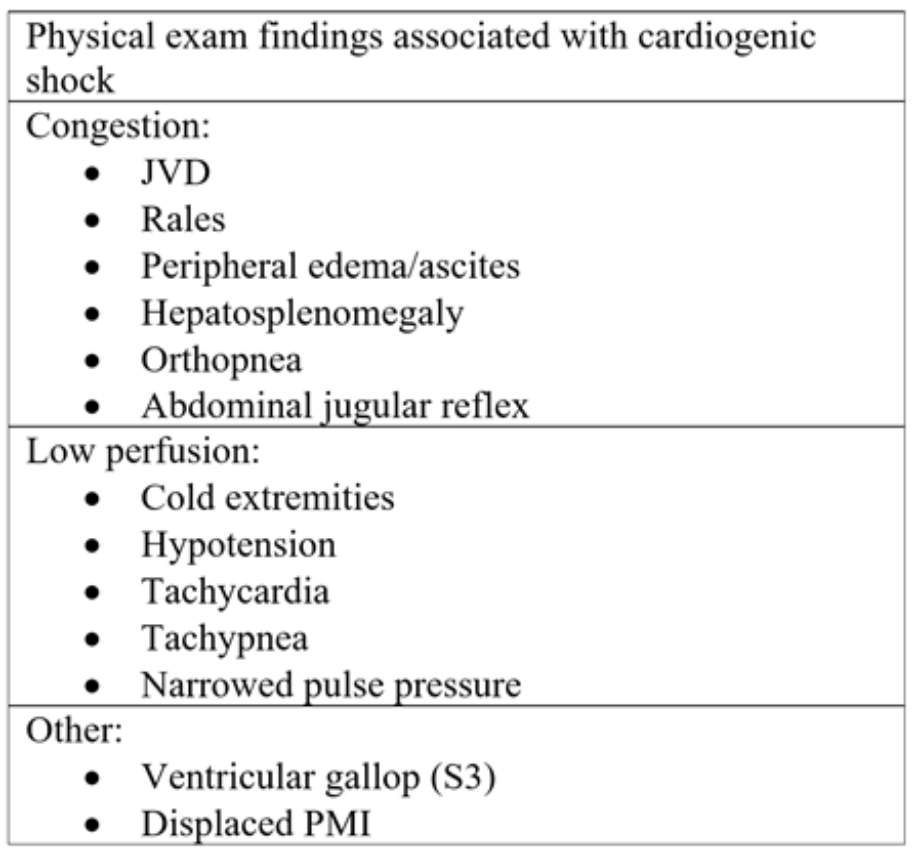
Taulukko 2: Akuutin sydämen vajaatoiminnan ja sitä seuraavan kardiogeenisen sokin aikana havaitut fyysisen kokeen komponentit. 18
Vaikka JVP on hyödyllinen välityspiste kohonneille kiilapaineille, 19 voi olla vaikea arvioida ruumiinhoidon ja potilaan sijainnin vuoksi (sängyn pään tulisi olla 45 astetta koholla, mikä voi olla vaikeaa vaikeaa ortopneaa sairastavilla potilailla). 20 JVP mitataan laskemalla korkein sykepiste senttimetreinä rintakehän yläpuolelle ja lisäämällä sitten 5 (koska oikea eteinen on 5 cm rintakehän alapuolella), mikä korreloi venytykseen cmH20: ssa (kuva 2). Korotettujen arvojen katsotaan usein olevan suurempia kuin 6-8 cmH20.18. Huomattavaa on, että kohonneeseen JVP: hen liittyy lisääntynyt kuolleisuusriski, suhteellisen riskin (RR) ollessa 1,52,18
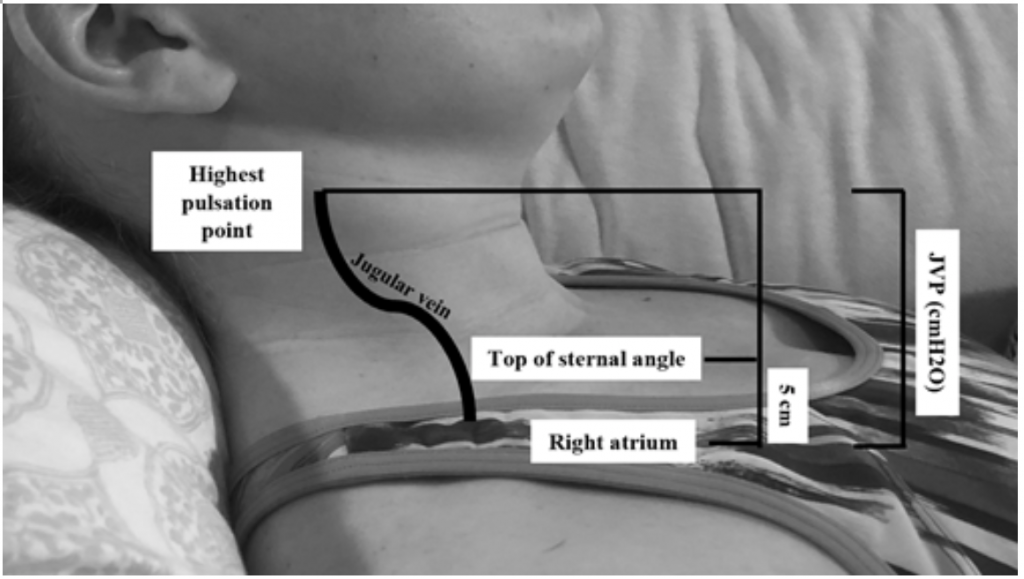
Kuva 2: JVP: n mittaaminen, sovitettu Shah & Cowgerilta (2014). 18
Labs saattaa näyttää metabolinen asidoosi (laktaatin lisääntyessä perifeerisen iskemian vuoksi), munuaisten hypoperfuusio, josta seuraa akuutti munuaisvaurio, ja mahdolliset todisteet sydämen iskemiasta, jossa on kohonneet troponiini- ja EKG-muutokset.15 CardShock-tutkimuksessa 219 CS: n monikeskustutkimus, prospektiivinen, havainnointitutkimus potilailla laktaattitasot liittyivät merkittävästi lisääntyneeseen kuolleisuuteen (korjattu kerroinsuhde 1,4) .6 On tärkeää huomata, että laktaattitason nousu ei ole spesifistä sepsikselle ja se voidaan havaita missä tahansa hypoperfuusioituneessa tilassa, kuten CS.
Toisaalta nämä fyysisen kokeen havainnot ja hemodynaamiset parametrit eivät aina pidä paikkaansa. SHOCK Trial -rekisteriä käyttäneessä tutkimuksessa 5,2%: lla CS-potilaista ei ollut selkeää hypotensiota, vaikka heillä oli merkkejä perifeerisestä hypoperfuusiosta ja matalasta CI: stä. SVR) ja ylläpitää väliaikaisesti verenpainetta, tosin yleensä kapealla pulssipaineella.22 Jopa potilailla, joilla on kliinisesti merkittävä keuhkopöhö kuvantamisen yhteydessä, voi esiintyä hengityksen vinkumista tai jopa selviä keuhkojen ääniä eikä kohinaa.23 Yhdessä tutkimuksessa keuhkojen ruuhkia havaittiin vain noin 2/3 sydäninfarktista, jotka ovat toissijaisia MI.21: n suhteen. Lisäksi, vaikka LV: n supistuvuus olisikin heikentynyt, CS-potilailla LVEF ei välttämättä vähene vakavasti. 14,24 Itse asiassa keskimääräinen EF CS-potilaiden kohortissa on noin 30%, mikä on pienentynyt, mutta odotettua suurempi.2
Vaikka tentti ei olekaan täydellinen, yksityiskohtainen fyysinen tentti, joka etsii ruuhkautumisen ja perifeerisen hypoperfuusion merkkejä, sekä elintoimintojen ja laboratorioiden huolellinen tarkastelu, voi olla ensimmäinen vihje, jolla potilaallasi on kardiogeeninen sokki.
Hoitopiste ECHO kardiogeenisen sokin arvioimiseksi
Kun potilaat ovat ED-verenpainetta alentavia tai hypoperfuusioituneita, RUSH-koe on nopea tapa erottaa sokki katsomalla ”pumppua, säiliö ja putket. ”25,26 CS: n tapauksessa transtorakaalinen kaikukardiogrammi osoittaa klassisesti hypodynaamisen, laajentuneen LV: n, jolla on huono LV-puristus ja siihen liittyvä mitraaliventtiilin etusivun riittämätön liike systolin ja diastolin aikana (ts. heikko supistuvuus). Ejektiofraktion (EF) ja CO: n (CO = aivohalvaustilavuus (SV) x syke (HR)) arviointi yksinkertaisesti ”silmämunan” LV-puristuksella on lääkäreiden riittävä arvio akuutissa ympäristössä.27 CS: ssä alempi vena cava (IVC), joka on epäsuora mittaus tehokkaasta intra verisuonitilavuuden, halkaisijan tulisi olla > 2 cm ja se romahtaa alle 50% sisäänhengitettynä. Nämä havainnot korreloivat kohonneen keskuslaskimopaineen kanssa.28 IVC-arviointi voi kuitenkin olla epätarkka, jos potilas on jo saanut vasodilataattoreita, diureetteja ja / tai on tuuletettu.29 Rintakehäikkunoissa on todennäköisesti keuhkoödeemaa liiallisen B: n muodossa. linjat (”keuhkiraketit”), jotka ovat seurausta välipohjan sakeutumisesta, joka johtuu veden kertymisestä interstitiumiin.30 Keuhkojen ruuhkautumisen lisäksi RUSH-tutkimuksessa voi olla keuhkopussin ja peritoneaalisen nesteen.25 Meta-analyysissä, jossa käytettiin tietoja kolmesta alkuperäisestä asiakirjoissa ja kahdessa tapausraportissa, RUSH-protokollan osoitettiin olevan sekä herkkä että spesifinen (vastaavasti 0,89 ja 0,97) CS.3: n diagnosoinnissa. 31 Huolimatta korkeasta tuloksena saadusta positiivisen todennäköisyyden suhteesta (LR) 22,29, vain kohtalainen negatiivinen LR on 0,17, mikä viittaa siihen, että RUSH-tentti ei ole täydellinen testi CS: n sulkemiseksi pois. Siksi RUSH-tenttiä tulisi käyttää huolellisen historia- ja fyysisen kokeen yhteydessä, eikä sitä tulisi käyttää yksin kardiogeenin diagnosointiin. c-shokki.
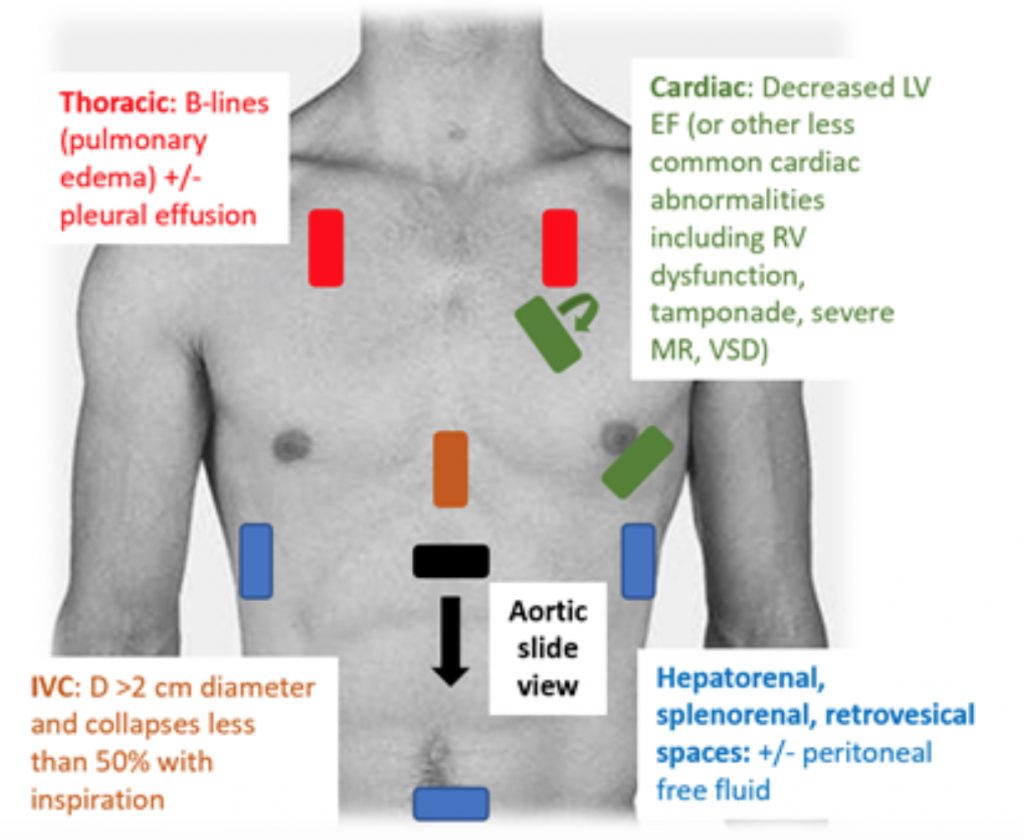
Kuva 3: RUSH-sängyn vieressä oleva USA: n tentti erilaistumattoman hypotension arvioimiseksi ja siihen liittyvät löydökset, jotka viittaavat CS.25: een , 26,29,30
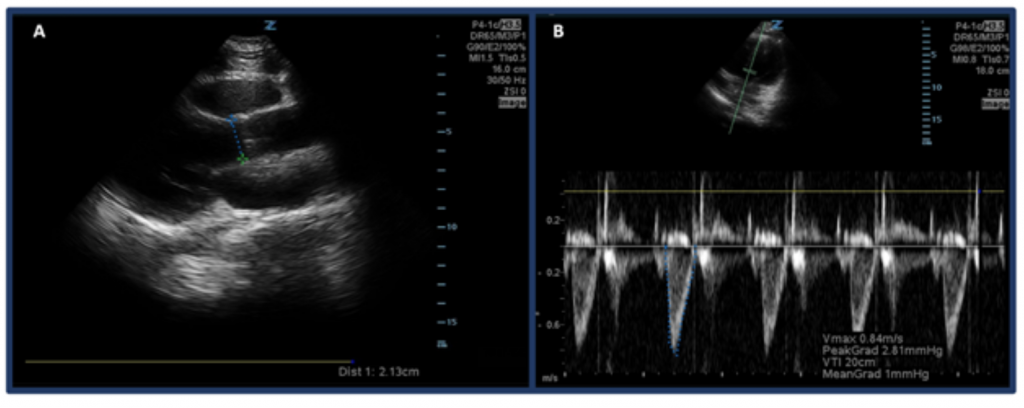
Sen sijaan, että arvioisit vain CO: n ”silmämunan kautta”, yksi tapa mitata CO ultraäänellä on ensin määrittää SV käyttämällä vasemman kammion ulosvirtauskanavan nopeuden aikaväliä (LVOT VTI, tai nopeudet veren virtaus aortan ulosvirtauskanavassa) ja LVOT-halkaisija. Erityisesti SV tai vasemman kammion kautta ulosheitetyn veren määrä lyöntiä kohden lasketaan LVOT: n VTI × LVOT: n poikkipinta-alalla .32 LVOT: n halkaisijan mittaamiseksi sijoita vaiheistettu matriisianturi parasternal pitkän akselin näkymään ja mittaa LVOT: n etäisyys juuri aortaventtiilin yläpuolella keskellä systolia. VTI mitataan apikaalisesta 5-kammiosta. Pulssiaaltodopplerimoodia käyttämällä doppleraaalto sijoitetaan juuri aortan venttiilin yläpuolelle ja doppleraajuuden muodot kirjataan. Muista kohdistaa akseli ulosvirtauskanavan kanssa parhaalla mahdollisella tavalla, jotta vältetään yli- / aliarvioinnit. Kun olet valinnut ”LVOT VTI” -mittaustyökalun, mittaa yhden poistoajan aaltomuoto. 33,34 Normaali LVOT-VTI vaihtelee välillä 18-22 cm, vaikkakin mahdollisesti pienempi HRs: n ollessa > 95 lyöntiä minuutissa. Potilailla, joilla on eteisvärinä, VTI-mittaukset ovat todennäköisesti todellisen arvon aliarviointeja, ja siksi keskimääräisen 3-5 peräkkäisen aaltomuodon ehdotetaan olevan keskimäärin.Jos voidaan odottaa, matalan LVOT-VTI: n ja haitallisten tulosten välillä on korrelaatio.32
Suositeltu arviointireitti
Kuten edellä on todettu, ei ole olemassa yhtä tutkimustulosta tai laboratoriotestiä, joka voi diagnosoida CS. Siksi, kun hypotensiossa tai hypoperfuusion oireissa on suuri epäily CS: stä, suosittelemme käyttämään historiaa, yksityiskohtaista fyysistä tutkimusta, Yhdysvaltain vieressä olevia laboratorioita (erityisesti kreatiniinia, laktaattia, troponiinia, BNP: tä ja muita hypoperfuusion merkkiaineita). / elinelinten vaurio) ja EKG (koska akuutti MI on ensisijainen syy CS: lle ja iskemian oireille ja saattaa vaatia revaskularisaatio) diagnoosin helpottamiseksi (katso kuva 5). Harkitse valtimon katetrimonitoria verenpaineeseen ja ohjaa hoitoa. Kohdennetun sydän- ja keuhkotutkimuksen lisäksi fyysisen kokeen tulee keskittyä JVD: hen ja raajojen perfuusioon. Edellä käsitelty RUSH-koe ja EF / CO / CI-arvon laskeminen LVOT VTI -mittausten avulla ovat arvokkaita lisäyksiä arviointiin. Kattavan lähestymistavan käyttäminen CS: n arvioimiseksi luo paremman käsityksen tästä heterogeenisesta taudista ja auttaa ohjaamaan hoitoa.
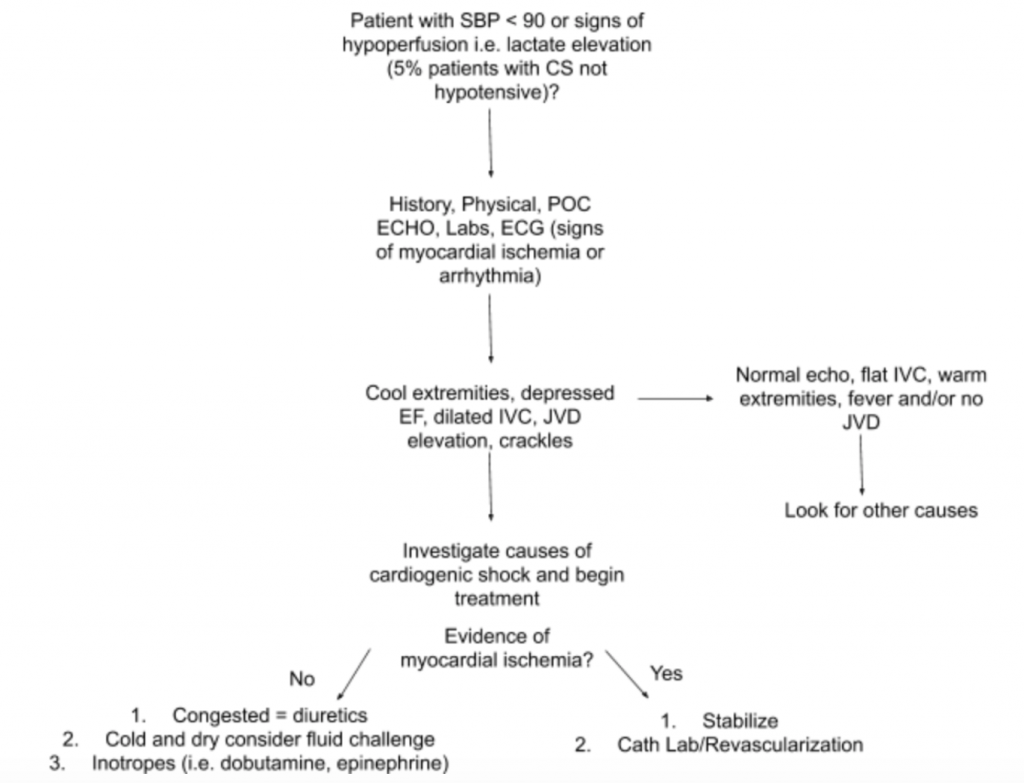
Tapauspäätelmä : Lisäarvioinnin jälkeen potilaan kaulalaskimon paine kohotetaan arvoon 10 cmH20 ja hänen jalkansa ovat viileitä viivästyneellä kapillaarien täyttämisellä. Bedside RUSH -testi osoittaa kahdenvälisen diffuusin keuhkopöhön ja arvioidun matalan EF-arvon.LVOT VTI mitataan vain 10 cm: ssä. EKG näyttää ST-korkeuksia etummaisissa johtimissa. Laktaatti ja troponiini ovat lievästi koholla. Potilas vakiintuu lyhyellä dobutamiini-, IV-furosemidi- ja CPAP-kokeella, jonka vitamiinit ja hengitystila paranevat kohtalaisesti, ja lähetetään sen jälkeen katolaboratorioon potentiaalista PCI: tä varten.
Ota kotipisteet:
- CS: n aiheuttaa pääasiassa akuutti sydäninfarkti (~ 70%) ja se on useimpien tutkimusten painopiste, mutta myös muut syyt on otettava huomioon (ks. täydellinen luettelo kuvassa 1).
- CS: lle toissijainen kuolleisuus on edelleen korkea (~ 60%), vaikka varhainen tunnistaminen ja puuttuminen parantavat selviytymistä.
- Suorita huolellinen fyysinen koe etsimällä hypoperfuusioita ja ruuhkia. JVP on tärkeä fyysisen kokeen komponentti CS: n diagnosoinnissa ja liittyy lisääntyneeseen kuolleisuuteen (RR = 1,52).
- RUSH-koe on sekä herkkä että spesifinen (vastaavasti 0,89 ja 0,97). CS. Yläpuolella tapahtuvaa ultraääntä tulisi toistaa usein, koska useimmat potilaat eivät ole aluksi läsnä CS: ssä. Ehdotettu lähestymistapa potilaiden arvioimiseksi, joilla epäillään keuhkoahtaumatautia, keskittyen sen heterogeeniseen patologiaan ja esitykseen, on esitetty yhteenvetona kuvassa 5.
FOAMed Resources:
- EM in 5 : Shock
- emDocs: Cardiogenic Shock
- emDocs: Sydämen vajaatoiminnan ED-hallinta – helmet ja karikot
- emDocs: RUSH (”Rapid Ultrasound for Shock”) -protokolla
- emDocs: Hypotensiivinen ED-potilas: peräkkäinen systemaattinen lähestymistapa
- Ensimmäiset 10 EM: erittelemätön hypotensio
