Miért mondják az emberek, hogy a víz szükséges az élethez? Miért nem találtunk soha olyan élő organizmust, amely virágozhatna teljesen száraz környezetben? Hogyan lehet, hogy valami szagtalan, színtelen, ízetlen és viszonylag reagálhatatlan a testtömegünk 60% -a? Miért nem lehet más folyadékot használni? Miért víz?
A víznek számos olyan tulajdonsága van, amelyek egyedivé teszik a vegyületek között, és lehetővé teszik az ismert élet minden formájának működését.
Ez az egyetlen természetes anyag, amely mindhárom fizikai állapotban megtalálható a természetes hőmérsékleten a Földön.
Ez azt jelenti, hogy a vizet folyadékként, a folyókban és tengerekben, szilárd anyagként, hóként és jégként, valamint gázként felhőként vagy gőzként látjuk. Ha ez nem így lenne, akkor a víz körforgása teljesen más lenne (mi lenne, ha a víz nem párologna el a napsütésben?); Előfordulhat, hogy hó és jég nem létezik (és fajok ezrei lennének hajléktalanok), és az időjárás nagyon eltérő lenne ( esne-e még?). Gondolhat bármi másra, ami más lenne? Gondolod, hogy még élhetnénk, ha a víz csak folyadék lenne a Földön természetesen előforduló hőmérsékleten? Mi a helyzet csak gázzal / szilárd anyaggal?
A jég kevésbé sűrű, mint a víz
Ez csak azt jelenti, hogy a jég a vízen úszik, és a tavak felülről lefelé fagynak le. Ez egyértelműen fontos a jégen élő állatok számára, mivel élőhelyeik jelentősen lecsökkennének vagy nem léteznének Egyáltalán, ha süllyedne a jég. Hasonlóképpen a halak és a tó életét is érintené, ha a tavak és tavak alulról felfelé fagynának be – a tó tetején lévő fagyasztott vízréteg némi szigetelést biztosít, és megakadályozza, hogy a többi víz lehűljön. gyorsan.Ezt úgy teszi, hogy gátat szab a hidegnek levegő és az alatta lévő víz. Ez azt jelenti, hogy a nagy víztestek nem fáznak olyan mélyen a mélyben, mint amilyen lehet, ha a jég elsüllyed, és segít a vadon élő állatoknak a tavakban túlélni a tél folyamán. Valójában a víz sűrűbbé válik, és addig hűtik, amíg el nem éri a $ 4 ^ \ circ $ értéket. C (amelyet a thegraph-on láthat), utána ismét kevésbé sűrűsödik. A legtöbb anyag hűlés közben fokozatosan sűrűbbé válik. Az alábbi grafikon azt mutatja be, hogy a víz sűrűsége hogyan változik a hőmérséklettel.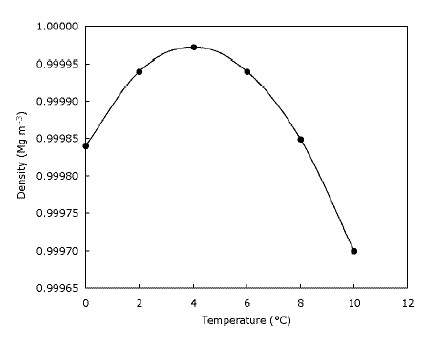
A víz nagyon magas olvadás- és forrásponttal rendelkezik, összehasonlítva más hasonló molekulákkal
Ez azt jelenti, hogy szilárd anyagként, folyadékként és gázként tekintik a Földön. Ha a víz nem folyadék a legtöbb hőmérsékleten, amelyet a Földön látunk, a tengerek mind jégek lennének, nem lenne eső, nincs mit gyűjteni a növényeknek és az italokat inni. Még sejtjeink is folyékony vízzel vannak megtöltve, ami szintén nem lenne lehetséges.
Úgy hívják, hogy “univerzális oldószer”, mert képes annyi anyag oldására.
A testünkben lévő víz i Többnyire sejtjeinkben vannak, ahol tiszta alakot ad nekik, valamint hasznos molekulák milliárdjait oldják fel benne. Sejtjeinket vízzel kell betölteni, hogy megfelelően működjenek, mert a bennük lévő enzimek csak oldatban működnek. A víz testünkben is a közlekedés útján történik “a vér többnyire víz, oldott hormonok és gázok vannak benne, valamint toxinok, például karbamid, amelyek még több vízzel távoznak a testből. A vízben történő szállítás sokkal kisebb skála: ha valami feloldódik, akkor mozoghat az oldószerben. Például, ha egy enzimnek kalciumionokra van szüksége az aktiváláshoz, és elkezd dolgozni, akkor ezeknek megfelel, amikor a sejt belsejében lévő oldatban mozognak. kalcium mennyisége a sejtben, annál valószínűbb, hogy az enzim hamarabb találkozik egy ionral. Megismerhette a diffúziót és az ozmózist is, amelyek kulcsfontosságú fogalmak a sejtek működésének megértésében és a víz jelenlétére való támaszkodásában. hőkapacitás.
Bár ez az ötlet kissé megfélemlítőnek tűnik, valójában nagyon egyszerű – annyit jelent, hogy sok energiára van szükség ahhoz, hogy a víz kissé melegebb legyen. Ezért egy forró napon a homok a tengerparton túl meleg lehet a járáshoz de a tenger még mindig hűvös; a nap energiája elegendő ahhoz, hogy sokat melegítsen a homokban, a víz azonban csak keveset. Ennek nagyon fontos következményei vannak, különösen a vízben élő szervezetekre nézve. A tengerek, tavak és folyók sokkal állandóbb hőmérsékletet tartanak, mint a levegő, ami azt jelenti, hogy az állatok egész évben vízben élhetnek anélkül, hogy alkalmazkodniuk kellene a nagy hőmérsékleti változásokhoz (szerinted mi történne, ha a víz könnyebben lehűlne? Milyen problémákat okozhat ez? jelentenek egy kis tóban élő organizmusoknak?). Ez azt is jelenti, hogy a testhőmérsékletünket meglehetősen nehéz gyorsan megváltoztatni, és ezáltal sokkal könnyebbé teszi agyunk feladata az állandó testhőmérséklet fenntartása (Mi történhet, ha testhőmérsékletünk gyorsan és könnyen megváltozik?).
Felületi feszültség
Talán észrevette, hogy ha egy tűt helyez egy tál víz felszínére, az lebeg, de ha bedobja, akkor megsüllyed.Ennek oka, hogy a tű sűrűbb, mint a víz, ezért süllyedni akar, de a víz felületi feszültsége tartja fenn. A felületi feszültség olyan tulajdonság, amely azt jelenti, hogy a víz felülete nem akar megtörni – “ragadós”. Ezt akkor is láthatja, amikor egy csészét a széléig megtölt, mivel a víz felszíne összetart és ellenáll a kiömlésnek. A víz nagy felületi feszültsége az oka annak, hogy egyes legyek süllyedés nélkül landolhatnak a felszínén. Ez a koncepció nagyon szorosan kapcsolódik egy másikhoz, a kapilláris működés eszméjéhez.
Kapilláris cselekvés
A felületi feszültséghez hasonlóan ez a vízmolekulák “összetapadásának” gondolata körül forog. Ha nagyon finom csövet tesz egy főzőpohárba, akkor látni fogja, hogy a víz egy része rövid úton halad felfelé a csövön; ezt kapilláris hatásnak nevezik, és az okozza, hogy a víz a cső oldalához és a víz más molekuláihoz tapad, és magával húzza őket a csövön. Végül a felhúzott víz súlya túl nagy ahhoz, hogy meg lehessen támasztani, és a víz abbahagyja az egyensúlyt. Ugyanez az elv lehetővé teszi a növények számára, hogy a talajból vizet szívjanak fel; amint a vízmolekulák felfelé haladnak a száron, több vízmolekula tapad rájuk, és egyre inkább ragaszkodik azokhoz és így tovább, amíg egy vízoszlopot szállítanak a xilemben (erről többet megtudhat, keresse meg a “transzpirációt”).
De miért?
A víz ezen tulajdonságai kritikus fontosságúak az élet számára, mivel ismerjük, de miért van a vízben? Senki más szubsztancia sem csinálja ezeket a dolgokat? Mi az a víz, ami miatt más? A kérdésekre adott válaszok megértéséhez tanulmányoznia kell a víz molekulaszerkezetét. A víz kémiai képlete H2O, ami azt jelenti, hogy két hidrogénatomot tartalmaz, amelyek kovalensen kapcsolódnak az egy oxigénatomhoz, így: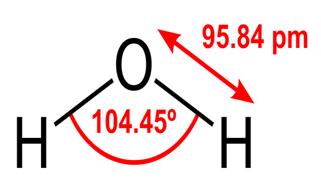
A 95.84pm mutatja a víz hosszát. kötés az oxigén és a hidrogén között; egy óra rövid a pikométer, ami egy billióméter méter. A bemutatott szög a két hidrogénmag közötti hegyes szög (van valami ötlete arról, hogy miért nem “t $ 180 ^ \ circ $? Miért legyen $ 180 ^ \ circ $?”) Ez a diagram a kötéseket vonalakként ábrázolja, amelyek úgy néz ki, mintha minden pontban azonosak lennének? ez nem így van. Mivel az oxigén elektronegatívabb, mint a hidrogén, az OH-kötésben lévő elektronokat vonzza maga felé. Ha a vonal vastagsága az elektron sűrűségét képviseli (az elektronok időtartamát) a kötés ezen részén töltik), az OH-kötés valójában inkább így néz ki:
KÉP a kötés polarizációját mutatja
Amint láthatja, az elektronok idejük nagy részét az oxigénmaghoz közelebb töltik. az oxigén kissé negatív töltésű, és hogy a hidrogének kissé pozitívan töltődnek fel. Ezt polaritásnak nevezzük, és ez a víz fogalmának legfontosabb fogalma
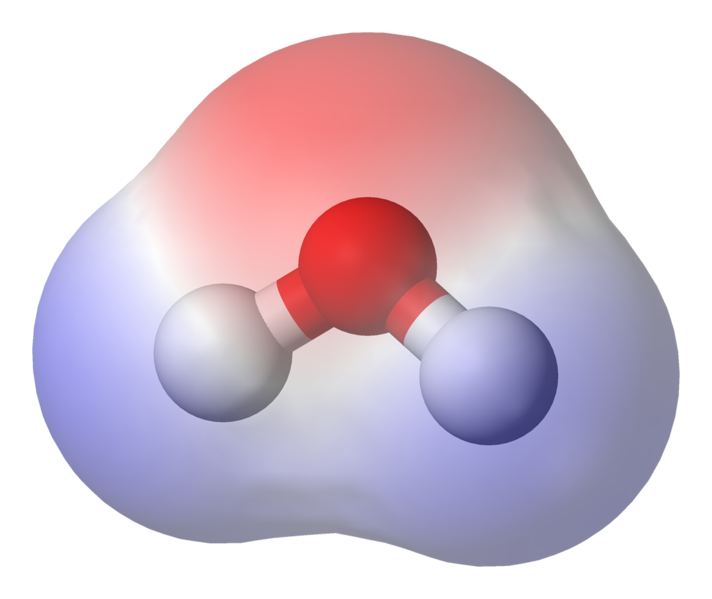
Ez azt jelenti, hogy n között gyenge ionos kölcsönhatások léphetnek fel nyolcvizű vízmolekulák, mivel az egyik molekula kissé pozitív hidrogénje vonzódik a másikban kissé negatív oxigénhez. Ezeket hidrogénkötéseknek nevezzük.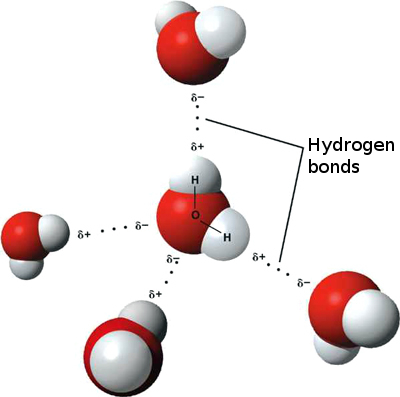
Ezért a víz “tapad” önmagához, nagy felületi feszültséget és kapilláris hatással történő mozgásképességet biztosítva.
A hidrogénkötések lebontásához nagy energiára van szükség, ezért magas a víz olvadáspontja és forráspontja, és ezért magas a fajlagos hőteljesítménye.
Az anyag vízben oldódik, ha poláros vagy ión. Ez azért oldódik fel, mert hidrogénkötéseket képez a vízzel. Az olaj nem poláros, ezért nem oldódik fel. A só, a NaCl, feloldódik, mert ionos. Gondolna néhány más, vízben oldódó anyagra? Hogyan képeznek hidrogénkötéseket vele? Tud-e hasonló képet rajzolni az alábbihoz, bemutatva, hogy a glükóz miért oldódik? Többé-kevésbé oldódik vízben, mint a só? Miért gondolja ezt?
Ábra arról, hogy mi történik az oldatban lévő NaCl-val:
