사람들은 왜 물이 생명에 필요하다고 말합니까? 완전히 건조한 환경에서 번성 할 수있는 살아있는 유기체를 찾지 못한 이유는 무엇입니까? 무취, 무색, 무미, 상대적으로 반응이없는 것이 우리 체질량의 60 %를 차지하는 이유는 무엇입니까? 다른 액체를 사용할 수없는 이유는 무엇입니까? 물은 왜 물인가?
물은 화합물 사이에서 독특하고 알려진 모든 형태의 생명체가 기능 할 수 있도록하는 몇 가지 특성을 가지고 있습니다.
자연적으로 발생하는 온도에서 세 가지 물리적 상태 모두에서 발견되는 유일한 천연 물질입니다. 이것은 우리가 물을 액체로, 강과 바다에서 고체로, 눈과 얼음으로, 가스로, 구름 또는 증기로 본다는 것을 의미합니다. 그렇지 않다면 물의 순환이 완전히 달라졌을 것입니다 (물이 “태양에서 증발하지 않았다면 어떨까요?”). 눈과 얼음이 존재하지 않을 수도 있고 (이제 수천 종의 노숙자가 될 것입니다) 날씨가 매우 다를 것입니다 ( 아직 비가 올까요?). 다른 것이 생각 나지 않나요? 지구에서 자연적으로 발생하는 온도에서 물이 액체 일 뿐이라면 우리가 살 수 있다고 생각하나요? 가스 / 고체 만은 어떻습니까?
얼음은 물보다 밀도가 낮습니다.
얼음이 물에 뜨고 호수가 위에서 아래로 얼어 붙는다는 뜻입니다. 얼음 위에서 사는 동물에게는 서식지가 크게 줄어들거나 존재하지 않기 때문에 이는 분명히 중요합니다. 얼음이 가라 앉는 경우 비슷하게, 호수와 연못이 바닥에서 위로 얼면 물고기와 다른 연못 생활에 영향을 미칠 것입니다. 연못 상단의 얼어 붙은 물 층은 약간의 단열 효과를 제공하고 나머지 물이 차가워지는 것을 방지합니다. 추위 사이에 장벽을 만들어서 공기와 아래의 물. 이것은 큰 물이 얼음이 가라 앉을 때처럼 빨리 깊어지지 않고 겨울 동안 연못에서 야생 동물이 살아남을 수 있도록 도와 준다는 것을 의미합니다. 실제로 물이 더 조밀 해지면 $ 4 ^ \ circ $에 도달 할 때까지 냉각됩니다. C (그래프에서 볼 수 있음) 이후 다시 밀도가 낮아집니다. 대부분의 물질은 냉각되면서 점차 밀도가 높아집니다. 아래 그래프는 온도에 따라 물의 밀도가 어떻게 변하는 지 보여줍니다.
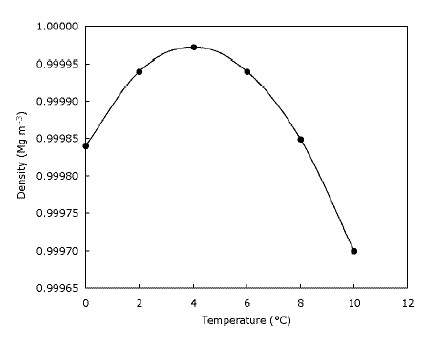
물은 다른 유사한 분자에 비해 녹는 점과 끓는점이 매우 높습니다.
이것은 지구상에서 고체, 액체 및 기체로 간주된다는 의미입니다. 물이 아닌 경우 지구상에서 볼 수있는 대부분의 온도에서 액체 바다는 모두 얼음이 될 것이고, 비가 내리지 않을 것이며, 식물이 모을 수 있고 동물이 마실 수 없을 것입니다. 우리 세포조차도 액체 물로 채워져있을 것입니다. br> 많은 물질을 녹일 수 있기 때문에 “유니버설 솔벤트”라고 불립니다.
우리 몸의 물 i 주로 우리 세포에 포함되어 있으며, 세포에 투명한 모양을 제공하고 수십억 개의 유용한 분자가 용해되어 있습니다. 세포 내부의 효소는 용액에서만 작동하기 때문에 세포가 제대로 작동하려면 물로 채워야합니다. 물은 또한 우리 몸에서 수송이 일어나는 수단이기도합니다. “혈액은 대부분 물이며 초기에 용해 된 호르몬과 가스뿐만 아니라 더 많은 물로 몸에서 제거되는 요소와 같은 독소를 가지고 있습니다. 훨씬 작은 규모 : 어떤 것이 용해되면 용매 내에서 움직일 수 있습니다. 예를 들어, 효소가 활성화되고 작동을 시작하기 위해 칼슘 이온이 필요한 경우 세포 내부의 용액에서 이동하면서 이들을 만나게됩니다. 세포 내 칼슘의 농도가 높을수록 효소가 더 빨리 이온을 만날 가능성이 높습니다. 또한 세포가 기능하고 물의 존재에 의존하는 방식을 이해하는 데 핵심 개념 인 확산 및 삼투에 대해 배웠을 것입니다.
물은 높은 특이성을가집니다. 열용량.
이 아이디어가 약간 겁나게 들리지만 실제로는 매우 간단합니다. 물을 조금 더 따뜻하게 만드는 데 많은 에너지가 필요하다는 의미입니다. 더운 날 해변에 모래가있는 이유입니다. 걷기에는 너무 더울 수 있습니다 하지만 바다는 여전히 시원합니다. 태양의 에너지는 모래를 많이 데우기에 충분하지만 물은 아주 조금만 있습니다. 이것은 특히 물에 사는 유기체에게 매우 중요한 의미를 가지고 있습니다. 바다, 호수, 강은 공기보다 훨씬 더 일정한 온도를 유지합니다. 즉, 동물은 큰 온도 변화에 적응하지 않고도 일년 내내 물 속에서 살 수 있습니다 (물이 더 쉽게 식 으면 어떻게 될 것이라고 생각합니까? 어떤 문제가 발생할 수 있습니까? 작은 연못에 사는 유기체에게 포즈를 취합니까?). 이것은 또한 우리의 체온이 빠르게 변하기가 상당히 어렵고 따라서 우리의 뇌가 일정한 체온을 유지하는 일을 훨씬 쉽게 만든다는 것을 의미합니다 (체온이 빠르고 쉽게 변하면 어떻게 될까요?).
표면 장력
물이 담긴 그릇의 표면에 바늘을 대면 물에 뜨지 만 그 속에 던져 넣으면 가라 앉는 것을 눈치 채 셨을 것입니다.바늘이 물보다 밀도가 높기 때문에 가라 앉고 싶지만 물의 표면 장력에 의해 고정되기 때문입니다. 표면 장력은 물의 표면이 깨지기를 원하지 않는다는 것을 의미하는 속성입니다. 컵을 가장자리까지 채울 때도이를 볼 수 있습니다. 물 표면이 서로 붙잡고 흘리지 않기 때문입니다. 물의 높은 표면 장력은 일부 파리가 가라 앉지 않고 표면에 착륙 할 수있는 이유입니다. 이 개념은 모세관 작용이라는 또 다른 개념과도 매우 밀접하게 관련되어 있습니다.
모세관 작용
표면 장력과 유사하게 이것은 물 분자가 서로 “붙어”있다는 생각을 중심으로합니다. 아주 미세한 튜브를 물 비이커에 넣으면 물의 일부가 튜브 위로 짧은 길로 이동하는 것을 볼 수 있습니다. 이것을 모세관 작용이라고하며, 물이 튜브의 측면과 다른 물 분자에 달라 붙어 튜브를 끌어 당겨서 발생합니다. 결국 끌어 당기는 물의 무게가 너무 커서지지 할 수없고 물은 평형에 도달 한 상태에서 움직이지 않습니다. 이 같은 원리는 식물이 땅에서 물을 끌어 올릴 수있게합니다. 물 분자가 줄기 위로 이동함에 따라 더 많은 물 분자가 그들에 달라 붙고 더 많은 물 분자가 목부에서 물기둥이 운반 될 때까지 더 많이 붙습니다 (이에 대해 자세히 알아 보려면 “증산”을 찾아보십시오).
그런데 왜?
우리가 아는 것처럼 물의 이러한 모든 속성은 생명에 중요한데 왜 물이 가지고있는 것일까 요? 다른 물질도 이러한 일을하지 않습니까? 물을 다르게 만드는 것은 무엇입니까? 이러한 질문에 대한 답을 이해하려면 물의 분자 구조를 연구해야합니다. 물의 화학식은 H2O입니다. 즉, 다음과 같이 하나의 산소 원자에 공유 결합 된 두 개의 수소 원자를 포함합니다.
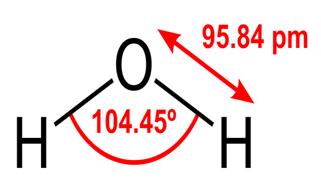
95.84pm은 물의 길이를 나타냅니다. 산소와 수소 사이의 결합; 1pm은 1 조분의 1 미터 인 picometre의 줄임말입니다. 표시된 각도는 두 개의 수소 핵 사이의 예각입니다 (왜 이것이 $ 180 ^ \ circ $가 아닌지에 대한 아이디어가 있습니까? 왜 $ 180 ^ \ circ $이되어야합니까?)이 다이어그램은 결합을 선으로 나타냅니다. 산소는 수소보다 전기 음성이 더 높기 때문에 OH 결합의 전자를 자기쪽으로 끌어 당깁니다. 선의 두께가 전자 밀도를 나타내는 경우 (전자가 시간의 양) OH 결합은 실제로 다음과 같이 보입니다.
결합의 분극화를 보여주는 사진
전자가 대부분의 시간을 산소 핵에 더 가깝게 보냅니다. 산소는 약간 음전하를 띠고 수소는 약간 양전하를 띠고 있습니다. 이것을 극성이라고하며 물의 특성에 숨겨진 핵심 개념입니다.
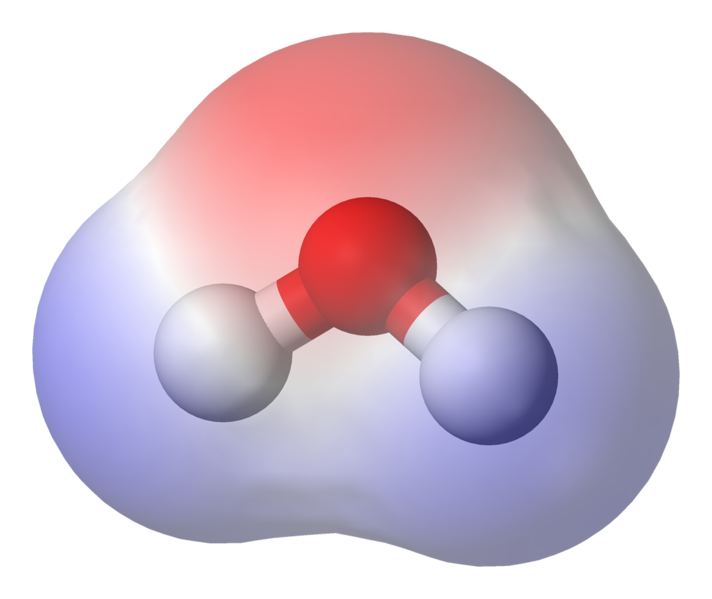
이것은 n 사이에 약한 이온 상호 작용이 발생할 수 있음을 의미합니다. 한 분자의 약간 양의 수소가 다른 분자의 약간 음의 산소에 끌리기 때문에 주변 물 분자. 이를 수소 결합이라고합니다.
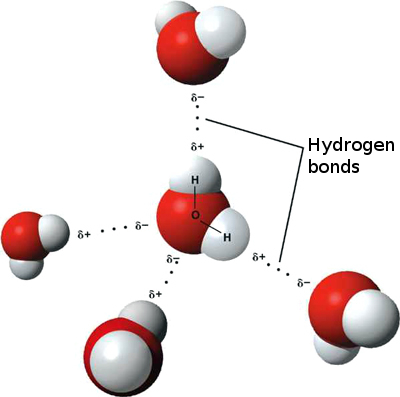
물이 자체에 “고착”되어 높은 표면 장력과 모세관 작용에 의해 움직일 수있는 능력을 부여하는 이유입니다.
수소 결합을 분해하려면 많은 에너지가 필요하기 때문에 물의 녹는 점과 끓는점이 높고 비열 용량이 높은 것입니다.
물질이 극성이거나 이온. 물과 수소 결합을하여 용해되기 때문입니다. 기름은 극성이 아니기 때문에 용해되지 않습니다. 소금 인 NaCl은 이온이기 때문에 용해됩니다. 물에 녹는 다른 물질을 생각할 수 있습니까? 그들은 어떻게 수소 결합을 형성합니까? 포도당이 용해되는 이유를 보여주는 아래 그림과 비슷한 그림을 그릴 수 있습니까? 소금보다 물에 어느 정도 용해됩니까? 왜 이것이라고 생각하십니까?
솔루션에서 NaCl에 어떤 일이 발생하는지 다이어그램 :
