Newsflash
Newsflash přerušuje váš oblíbený televizní program. „V první národní bance došlo k zadržení. Podezřelý uprchl v autě a předpokládá se, že je někde v centru města. Všichni jsou požádáni, aby byli ve střehu.“ Lupič může být lokalizován pouze v určité oblasti – policie nemá přesné místo, pouze obecnou představu o tom, kde se zloděj nachází.
V roce 1926 Rakouský fyzik Erwin Schrödinger (1887–1961) použil dualitu vlnových částic elektronu k vývoji a řešení složité matematické rovnice, která přesně popsala chování elektronu v atomu vodíku. Kvantově mechanický model atomu pochází z řešení k Schrödingerově rovnici. Kvantizace elektronových energií je požadavkem k vyřešení rovnice. Je to na rozdíl od Bohrova modelu, ve kterém se kvantifikace jednoduše předpokládala bez matematického základu.
Připomeňme si, že v Bohrově modelu přesná dráha elektronu byla omezena na velmi dobře definované kruhové dráhy kolem jádra. Kvantově mechanický model je od toho radikálním odklonem. Řešení Schrödingerovy vlnové rovnice, zvané vlnové funkce, dávají pouze pravděpodobnost nalezení elektronu v daném bodě kolem jádra. Elektrony nepochodují kolem jádra po jednoduchých kruhových drahách.
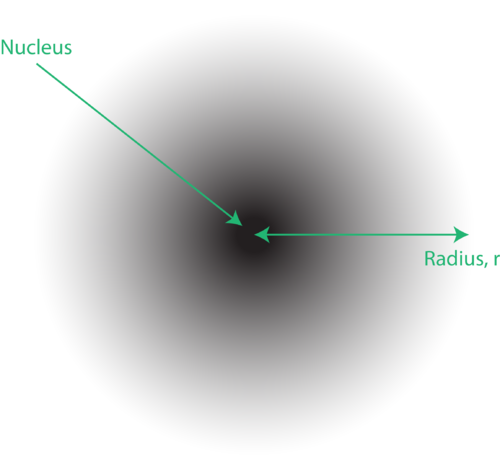
Obrázek 1. An elektronový mrak: tmavší oblast blíže k jádru naznačuje vysokou pravděpodobnost nalezení elektronu, zatímco světlejší oblast dále od jádra naznačuje nižší pravděpodobnost nalezení elektronu.
Umístění elektronů v kvantově mechanickém modelu atomu se často označuje jako elektronový mrak. Na elektronový mrak lze myslet následujícím způsobem: Představte si, že na podlahu umístíte čtvercový kus papíru s tečkou v kruhu představujícím jádro. Nyní vezměte značku a opakovaně ji pusťte na papír, přičemž v každém bodě značky zasáhne malé značky. Pokud značku mnohokrát upustíte, bude celkový vzor teček zhruba kruhový. Pokud míříte směrem ke středu přiměřeně dobře, bude v blízkosti jádra více teček a postupně méně bodů, když se od něj vzdálíte. Každá tečka představuje místo, kde by mohl být elektron v daném okamžiku. Kvůli principu nejistoty neexistuje způsob, jak přesně zjistit, kde je elektron. Elektronový mrak má proměnné hustoty: vysokou hustotu, kde je nejpravděpodobnější elektron, a nízkou hustotu, kde je nejpravděpodobnější elektron (obrázek 1).
Aby bylo možné konkrétně definovat tvar mrak, je obvyklé označovat oblast vesmíru, ve které je 90% pravděpodobnost nalezení elektronu. Tomu se říká orbitál, trojrozměrná oblast vesmíru, která označuje, kde je vysoká pravděpodobnost nalezení elektronu.
Shrnutí
- Schrödingerova vlna rovnice nahradila Bohrovy představy o umístění elektronů faktorem nejistoty.
- Umístění elektronu lze určit pouze jako pravděpodobnost, že se elektron nachází někde v určité oblasti.
Procvičování
Pomocí následujícího odkazu můžete odpovědět na následující otázky:
http://science.howstuffworks.com/atom8.htm
- Jaký byl jeden problém s Bohrovým modelem atomu?
- Co ukázal Heisenberg o elektronech?
- Co odvodil Schrödinger?
Recenze
- Co vyžaduje kvantově mechanický pohled na atom?
- Co je vlnová funkce?
- Co naznačuje elektronový mrak s vysokou hustotou?
glosář
- elektronový mrak: umístění elektrony v kvantově mechanický model atomu.
- orbitální: Trojrozměrná oblast vesmíru, která označuje, kde je vysoká pravděpodobnost nalezení elektronu.
- kvantově mechanický model: model atom, který je odvozen ze Schrödingerovy vlnové rovnice a zabývá se pravděpodobnostmi.
- vlnová funkce: Uveďte pouze pravděpodobnost nalezení elektronu v daném bodě kolem jádra.
