Reversibelt posterior leukoencefalopati syndrom (RPLS)
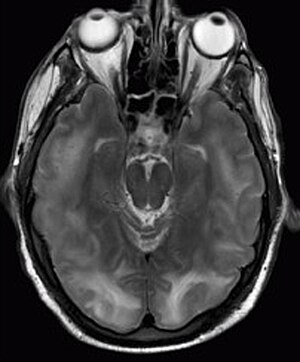
Posterior reversibel encefalopati syndrom synlig på magnetisk resonansavbildning som multipel kortiko -subkortikala områden av T2-viktad hyperintense (vit) signal som involverar occipitala och parietala lober bilateralt och pons.
Neurologi
Krampanfall, huvudvärk, synstörningar, förändrat mentalt tillstånd, ibland svagheter i lemmarna eller oförmåga att tala
Intrakraniell blödning
Posterior reversibel encefalopati syndrom (PRES), även känd som reversibelt posterior leukoencefalopati syndrom (RPLS), är ett sällsynt tillstånd där delar av hjärnan påverkas av svullnad, vanligtvis som ett resultat av en underliggande orsak. Någon med PRES kan uppleva huvudvärk, synförändringar och kramper, och vissa utvecklar andra neurologiska symtom som förvirring eller svaghet i en eller flera extremiteter. Namnet på tillståndet innehåller ordet ”posterior” eftersom det huvudsakligen men inte enbart påverkar baksidan av hjärnan (parietal och occipital lobes). Vanliga bakomliggande orsaker är allvarligt förhöjt blodtryck, njursvikt, allvarliga infektioner, vissa mediciner, vissa autoimmuna sjukdomar och preeklampsi. Diagnosen ställs vanligtvis genom hjärnskanning (MRI) på vilka områden av svullnad som kan identifieras.
Behandlingen för PRES är stödjande: avlägsnande av orsaken eller orsakerna och behandling av någon av komplikationerna, såsom antikonvulsiva medel för anfall. PRES kan kompliceras av intrakraniell blödning, men detta är relativt sällsynt. Majoriteten av människor återhämtar sig helt, även om vissa kan uppleva några kvarvarande symtom. PRES beskrevs först 1996.
Tecken och symtom
PRES har vanligtvis en akut debut. De flesta med PRES upplever huvudvärk och kramper; många upplever också synförändringar, förvirring och sömnighet, svaghet i armen och / eller benet på ena sidan av kroppen (hemiplegi), svårigheter att prata eller mer sällan andra neurologiska symtom. De visuella förändringarna i PRES kan inkludera hemianopsi (oförmåga att se den vänstra eller högra delen av synfältet), suddig syn, brist på visuell medvetenhet på ena sidan, synhallucinationer och kortikalblindhet.
Krampanfall i ungefär två tredjedelar av fallen. Hos barn är detta fortfarande vanligare, 90%. Om kramper uppstår kan de vara fokala eller generaliserade. En liten andel utvecklar status epilepticus, där krampanfall inte kontrolleras med enkla åtgärder.
Orsaker
Orsaker som kan bidra till utvecklingen av PRES är: immunsuppression (speciellt för organtransplantation, t.ex. med takrolimus), svår infektion och / eller sepsis, kemoterapi, autoimmun sjukdom och preeklampsi. Högt blodtryck är ofta närvarande. På samma sätt har majoriteten av personer med PRES nedsatt njurfunktion och 21% får regelbunden hemodialys. I PRES-relaterat till läkemedel kan det gå ett intervall på veckor till månader mellan behandlingen inleds och utvecklingen av PRES. Efter en hematopoietisk stamcellstransplantation (benmärgstransplantation) är risken för PRES cirka 8%, medan risken är lägre (0,4-6%) efter en fast organtransplantation.
Följande autoimmuna tillstånd har varit visat sig associeras med PRES: trombotisk trombocytopen purpura (TTP), primär skleroserande kolangit (PSC), reumatoid artrit (RA), Sjögrens syndrom, polyarterit nodosa (PAN), systemisk skleros, systemisk lupus erythematosus (SLE), granulomatos med polyangiit ( GPA), Crohns sjukdom och neuromyelit optica (NMO), liksom hemolytisk-uremiskt syndrom (HUS). Ett antal andra föreningar har också rapporterats, inklusive några andra läkemedelsgrupper, blodtransfusion, förhöjda kalciumnivåer, minskade magnesiumnivåer, postpartum cerebral angiopati och missbrukande droger (kokain och amfetamin).
Det har föreslagits att PRES är identiskt eller nära besläktat med hypertensiv encefalopati, närvaron av neurologiska symtom hos personer med en hypertensiv nödsituation.
Mekanism
Även om den exakta mekanismen är PRES inte helt förstås, anses den vara relaterad till ett problem med hjärnans blodkärl. Det finns flera teorier om varför dessa blodkärl kan bli felaktigt permeabla och låta den omgivande hjärnvävnaden bli svullen. Den ”vasogena” teorin antar att extremt högt blodtryck övervinner den normala förmågan hos blodkärl i hjärnan att upprätthålla ett normalt hjärnblodflöde. Det överdrivna trycket skadar endotelskiktet och blod-hjärnbarriären, vilket leder till svullnad (ödem).Detta påverkar övervägande de ”bakre” delarna av hjärnan som är mer mottagliga. Den ”vasogena” teorin verkar förklara nästan 50% av fallen med PRES där blodtrycket hade varit kraftigt förhöjt. Det kallas också ”genombrottsteorin” eller ”hyperperfusionsteorin”. Denna teori förklarar inte ödem i många andra fall där blodtrycket har varit normalt eller till och med lågt. i själva verket tenderar ödem att vara svårare hos dem utan onormalt förhöjt blodtryck.
I PRES sekundärt till andra orsaker har blodkärlskadorna tillskrivits andra mekanismer. Den ”cytotoxiska” teorin antyder att det är direkt cellskada av toxiner (vanligtvis mediciner) som utfäller ödem. Den ”immunogena” teorin föreslår en roll för immunsystemet (specifikt T-celler). Vissa anser att de cytotoxiska och immunogena teorierna tillsammans är en enda ”giftig” teori. Det verkar finnas en roll av cytokiner för att orsaka endotel dysfunktion.
Slutligen, enligt ”neuropeptid / cerebral vasokonstriktion” teori, utlöser vissa specifika ämnen (endotelin 1, tromboxan A2) blodkärlkramp med resulterande kärlväggsskada och ödem. Den senare hypotesen stöds av det vanliga fyndet av diffusa blodkärlspasmer (vasokonstriktion) hos många personer med PRES, och bevisen för minskad perfusion, även om krampen också kan vara en följd av blodkärlskador snarare än orsaken. Vissa inkluderar därför vasospasm i den ”toxiska” teorin. Det anses troligt att dessa multipla mekanismer alla spelar en roll i utvecklingen av PRES.
Diagnos
Det finns inga formella diagnostiska kriterier för PRES, men det har föreslagits att PRES kan diagnostiseras om någon har utvecklat akuta neurologiska symtom (anfall, förändrat mentaltillstånd, huvudvärk, synstörningar) tillsammans med en eller flera kända riskfaktorer, typiskt utseende vid hjärnbildning (eller normal bildbehandling) och ingen annan alternativ diagnos. Vissa anser att avvikelserna måste visas vara reversibla. Om ländryggen punkteras kan detta visa ökade proteinnivåer men inga vita blodkroppar. Datortomografisökning kan utföras i första hand; detta kan visa vita ämnesområden med låg densitet i de bakre loberna.
Diagnosen ställs vanligtvis med magnetisk resonansavbildning av hjärnan. Resultaten som är mest karakteristiska för PRES är symmetriska hyperintensiteter på T2-vägd avbildning i parietal och occipital lobes; detta mönster är närvarande i mer än hälften av alla fall. FLAIR-sekvenser kan vara bättre på att visa dessa avvikelser. Några specifika andra sällsynta mönster har beskrivits: det överlägsna frontal sulcus (SFS) vattendragsmönstret, ett vattendragsmönster som involverar hela halvklotet (holohemisfäriskt) och ett centralt mönster med vasogent ödem i den djupa vita substansen, basala ganglier, talami, hjärnstammen pons. Dessa distinkta mönster korrelerar i allmänhet inte med beskaffenheten av symtomen eller deras svårighetsgrad, även om svår ödem kan tyda på en sämre prognos. Om utseendet inte är typiskt måste andra orsaker till symtomen och bildavvikelser övervägas innan PRES kan diagnostiseras definitivt. I många fall finns det tecken på sammandragning av blodkärlen (om angiografi utförs), vilket tyder på en möjlig överlappning med reversibelt hjärnkärlsammandragningssyndrom (RCVS). Diffusions-MR kan användas för att identifiera områden med cytotoxiskt ödem orsakade av dåligt blodflöde (ischemi) men det är inte klart om detta är prognostiskt relevant. Onormal skenbar diffusionskoefficient ses i cirka 20% av fallen.
I 10-25% av fallen med PRES finns det tecken på blödning vid neurobildning. Olika typer av blödningar kan förekomma: blödning i själva hjärnvävnaden (intraparenchymal blödning), sulkal subaraknoidalblödning och mikroblod.
Behandling
Det finns ingen direkt behandling för PRES, förutom avlägsnande eller behandling av någon underliggande orsak. Till exempel kan immunsuppressiv medicin behöva hållas kvar. 40% av alla personer med PRES är tillräckligt sjuka för att kräva intag av intensivvårdsavdelning för noggrann observation och behandling av komplikationer. De med kramper får antikonvulsiva medel.
Om det finns en hypertensiv nödsituation sänks blodtrycket med 20-30% med kontinuerlig infusion av ett blodtryckssänkande läkemedel med noggrann övervakning. Av tillgängliga blodtryckssänkande medel kan nitrater behöva undvikas eftersom det finns en oro för att detta kan förvärra PRES även när blodtrycket sänks. I PRES sekundärt till preeklampsi kan magnesiumsulfat administreras.
Prognos
Med adekvat behandling gör 70-90% av personer med PRES full återhämtning inom timmar till dagar. 8–17% av personer med PRES dör, även om detta inte alltid är en direkt konsekvens av PRES.Av dem som har kvarvarande symtom efter PRES beror detta till stor del på blödning. Icke-upplösning av MR-abnormiteter har kopplats till sämre resultat. Om PRES orsakades av preeklampsi är prognosen bättre än i PRES på grund av andra orsaker.
Faktorer som förutsäger sämre prognoser är personens ålder, nivån av C-reaktivt protein i blodet ( en markör för inflammation), förändrat mentaltillstånd vid diagnos och förändrade markörer för koagulation. Personer med diabetes kan ha ett sämre resultat och abnormiteter i corpus callosum vid MR har kopplats till sämre prognos. Vissa mönster på elektroencefalografi ( EEG) är också associerat med ett sämre utfall.
Efter en episod av PRES, även när det var associerat med krampaktivitet, är det bara en liten andel människor som fortfarande riskerar att pågå anfall och majoriteten kan så småningom sluta antikonvulsiv behandling.
Epidemiologi
Förekomsten (antal fall per år) av PRES är inte känd, men ökad användning av MR-undersökningar har lett till ökat igenkänning.
Historia
PRES beskrevs först 1996 i en grupp på 15 patienter identifierades i efterhand i dokumentationen från New England Medical Center i Boston och Hôpital Sainte Anne i Paris. Namnet reviderades år 2000 från ”leukencefalopati” till ”encefalopati” eftersom den förra föreslog att det bara påverkar hjärnans vita substans, vilket inte är fallet.
- ICD-10: I67.83
- ICD-9-CM: 348.39
- MeSH : D054038
- SjukdomarDB: 10460
