OBJETIVOS DE APRENDIZAJE
- Diferenciar entre sustrato y producto, y definir la ecuación química
- Definir metabolismo, síntesis (anabólica), descomposición (catabólica) y reacciones de intercambio
- Diferenciar entre reacciones reversibles y reacciones irreversibles
- Explicar la síntesis de deshidratación y las reacciones de hidrólisis
- Explique la relación entre monómeros y polímeros
Las reacciones químicas comienzan con una o más sustancias que entran en la reacción. Las sustancias de nuestras células y tejidos corporales que entran en la reacción se denominan sustratos. Las una o más sustancias producidas por una reacción química se denominan productos.
Las reacciones químicas se representan mediante ecuaciones químicas colocando el (los) sustrato (s) a la izquierda y los productos a la derecha. Los sustratos y productos están separados por una flecha (\ (\ rightarrow \)) que indica la dirección y el tipo de reacción. Por ejemplo, nuestro sistema digestivo descompone la lactosa, el azúcar que se encuentra en la leche, en dos azúcares más pequeños, glucosa y galactosa. En esta reacción, la lactosa es el sustrato y la glucosa y la galactosa son los productos. La ecuación química para esta reacción es:
Lactosa \ (\ rightarrow \) Glucosa + Galactosa
Verificación de conceptos, términos y hechos
Estudio Preguntas Escriba su respuesta en forma de oración (no responda con palabras sueltas)
1. ¿Cuál es la diferencia entre un sustrato y un producto?
2. ¿Qué es una ecuación química?
El metabolismo se refiere a la suma de todas las reacciones químicas que ocurren en un organismo vivo. Hay tres tipos principales de reacciones químicas importantes en la fisiología humana: síntesis (anabólica), descomposición (catabólica) e intercambio.
- En una reacción de síntesis (syn- = together; -thesis = «put , lugar, conjunto ”), dos o más moléculas de sustratos se unen covalentemente para formar una molécula de producto más grande.
Las reacciones de síntesis requieren energía para formar los enlaces. Una reacción de síntesis se suele simbolizar
A + B \ (\ rightarrow \) AB, donde A y B son los sustratos, y AB es el producto. Las reacciones de síntesis también se pueden llamar actividades anabólicas o constructivas en una célula. - En una reacción de descomposición (de off , away = -composition = «poniendo juntos,
arreglando»), los enlaces covalentes entre los componentes de una molécula de sustrato más grande se rompen para formar moléculas de producto más pequeñas. Las reacciones de descomposición liberan energía cuando se rompen los enlaces covalentes en el sustrato. Una reacción de descomposición a menudo se simboliza como AB \ (\ rightarrow \) A + B; donde AB es el sustrato y A y B son los productos. Los diferentes tipos de reacciones de descomposición también pueden denominarse reacciones de digestión, hidrólisis, descomposición y degradación. Las reacciones de descomposición son la base de todas las actividades catabólicas o de ruptura en una célula. - En una reacción de intercambio, los enlaces covalentes se descomponen y luego se reforman de tal manera que los componentes de los sustratos se reorganizan para formar diferentes productos. Una reacción de intercambio a menudo se simboliza como AB + CD \ (\ rightarrow \) AC + BD. En esta reacción de intercambio, los enlaces covalentes entre A y B, y entre C y D se rompieron; y se formaron nuevos enlaces covalentes entre A y C, y B y D.


Verificación de conceptos, términos y hechos
Preguntas de estudio Escriba su respuesta en forma de oración (no responda con palabras sueltas)
1 . ¿Qué es una reacción de síntesis?
2. ¿Cómo se puede representar una reacción de síntesis usando letras?
3. ¿Qué es una reacción anabólica?
4. ¿Qué es una reacción de descomposición?
5. ¿Cómo se puede representar una reacción de descomposición usando letras?
6. ¿Qué es una reacción catabólica?
7. ¿Qué es una reacción de intercambio?
8. ¿Cómo se puede representar una reacción de intercambio usando letras?
9. ¿Qué es una reacción del metabolismo?
10. ¿Qué es el metabolismo?
Algunas reacciones metabólicas se denominan reacciones irreversibles. Esto significa que los productos
no se pueden cambiar o «revertir» de nuevo en sustratos. Estas reacciones están
representadas con una sola flecha, como en A + B \ (\ rightarrow \) C.
Por ejemplo:
Glucosa + Oxígeno \ (\ rightarrow \) Dióxido de carbono + Agua
Nota: Este es un tipo de reacción catabólica (la molécula de glucosa más grande se descompone moléculas de dióxido de carbono más pequeñas) relacionadas con la producción de energía celular. En las células animales, como los humanos, esta es una reacción irreversible.
Otras reacciones metabólicas se denominan reacciones reversibles. Esto significa que la reacción puede proceder de sustratos a producto (s) o de producto (s) a sustratos. El producto (s) se puede cambiar o «revertir» en sustratos. Se representan con una flecha doble como en A + B \ (\ leftrightarrow \) C + D.
Por ejemplo:
Glucógeno + Agua \ (\ leftrightarrow \) Glucosa
Nota: Cuando las células necesitan energía, el glucógeno (una molécula más grande utilizada como energía almacenar en algunas células) se pueden catabolizar a moléculas de glucosa más pequeñas, que luego se pueden catabolizar aún más para proporcionar energía para las funciones celulares. Cuando las células no necesitan tanta energía, o cuando los niveles de glucosa son muy altos, el glucógeno se sintetiza a partir de las moléculas de glucosa más pequeñas. Por ejemplo, las células musculares sintetizan glucógeno cuando están en reposo y catabolizan el glucógeno cuando se contraen. La forma en que procede esta reacción reversible depende de las necesidades corporales.
Verificación de conceptos, términos y hechos
Preguntas de estudio Escriba su respuesta en forma de oración (no responda usando palabras sueltas)
1. ¿Qué es una reacción reversible?
2. ¿Qué es una reacción irreversible?
En el cuerpo, las reacciones de síntesis (moléculas más pequeñas a moléculas más grandes, requieren energía) y reacciones de descomposición (moléculas más grandes a moléculas más pequeñas, liberan energía) a menudo se asocian con la formación y descomposición de moléculas de agua, respectivamente. Una reacción de síntesis por deshidratación es un tipo de reacción de síntesis que produce agua como subproducto. Una reacción de hidrólisis es un tipo de reacción de descomposición que utiliza agua.
En la síntesis de deshidratación (des = «off, remove»; hydrate = «water») que se muestra en la figura \ (\ PageIndex {2} \), dos monómeros se unen covalentemente en una reacción en la que uno cede un ion hidroxilo (-OH-) y el otro un ion hidrógeno (-H +). El monómero 1 y el monómero 2 son los sustratos de la izquierda, y los «monómeros unidos por un enlace covalente» es el producto de la derecha. El producto que se muestra aquí también se llama dímero (di- = dos, mer = parte). OH – y H + se combinan para formar una molécula de agua, que se libera como subproducto. Esto puede ser confuso porque el agua se produce durante la síntesis de deshidratación. El producto más grande se ha deshidratado (perdió el agua).
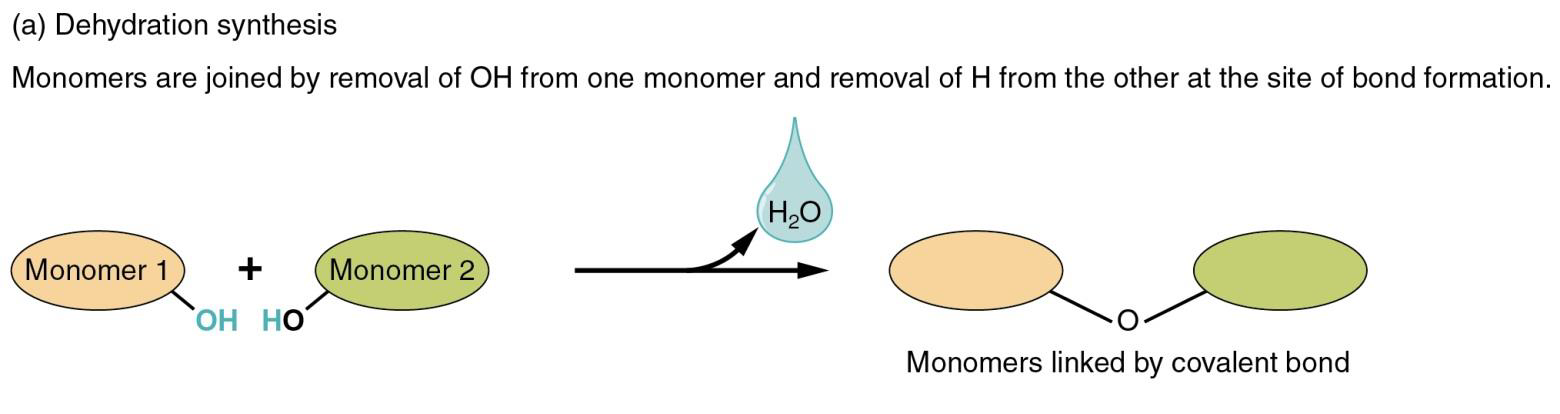
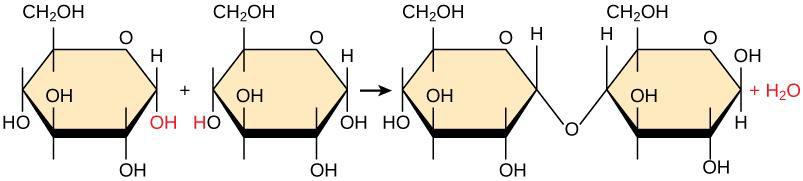
Figura \ (\ PageIndex {2} \) Ejemplo de síntesis de deshidratación: dos moléculas de glucosa (sustratos a la izquierda de la flecha) forman un enlace covalente para formar una molécula de maltosa (producto a la derecha de la flecha). El OH- y el H + que se muestran en rojo se combinan entre sí para formar H2O (que también se muestra en rojo)
En la reacción de hidrólisis que se muestra en la figura \ (\ PageIndex {3} \), (hidro- = «agua»; -lysis = «ruptura, un aflojamiento, una disolución») el enlace covalente entre dos monómeros se divide por la adición de un ion hidrógeno (H +) a uno y un ion hidroxilo (OH-) al otro. Estos dos iones provienen de la división de una molécula de agua, H2O, en H + y OH-. El dímero (monómeros unidos por un enlace covalente a la izquierda) es el sustrato, y el monómero 1 y el monómero 2 de la derecha son los productos.
Verificación de conceptos, términos y hechos
Preguntas de estudio Escriba su respuesta en forma de oración (no responda con palabras sueltas)
1. ¿Qué es una reacción de síntesis de deshidratación?
2. ¿Qué es una reacción de hidrólisis?
Las moléculas grandes compuestas por cientos o miles de átomos se denominan macromoléculas. Muchas macromoléculas están compuestas por unidades repetitivas del mismo bloque de construcción, similar a un collar de perlas que se compone de muchas perlas. Los polímeros (poly- = «muchos»; meros = «parte») son moléculas orgánicas grandes de cadena larga (macromoléculas) ensambladas a partir de muchas moléculas más pequeñas unidas covalentemente llamadas monómeros. Los polímeros consisten en muchas unidades monoméricas repetidas en cadenas largas, a veces con ramificaciones o entrecruzamiento entre las cadenas.
Tres de las cuatro clases de moléculas orgánicas identificadas previamente, es decir, carbohidratos, lípidos, proteínas y ácidos nucleicos. a menudo son polímeros hechos de subunidades de monómero más pequeñas (los lípidos no lo son). Por ejemplo, las proteínas son polímeros hechos de muchas moléculas más pequeñas unidas covalentemente, monómeros, llamados aminoácidos. Cada una de estas clases se considera con más detalle a continuación.
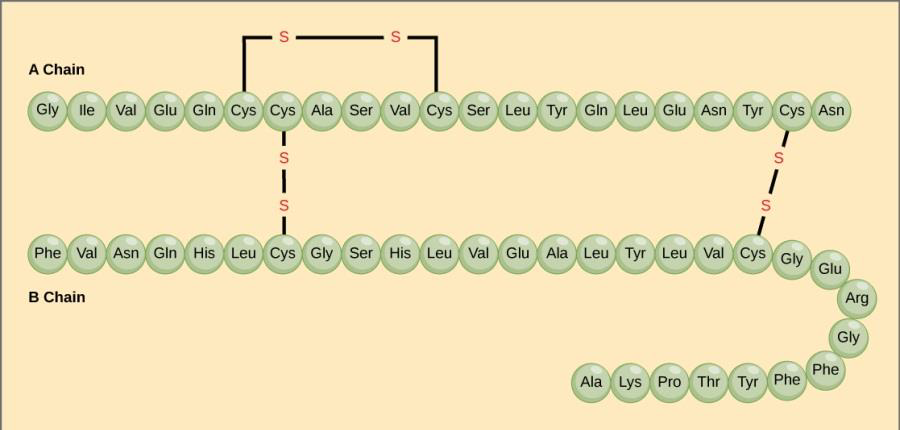
Figura \ (\ PageIndex {3} \) bidimensional vista de la proteína insulina. La insulina es un polímero hecho de monómeros unidos covalentemente llamados aminoácidos (mostrados como bolas verdes).
Verificación de conceptos, términos y hechos
Preguntas de estudio Escriba su respuesta en un forma de oración (no responda con palabras sueltas)
1. ¿Qué es un polímero?
2. ¿Qué es un monómero?
