Reversível síndrome de leucoencefalopatia posterior (RPLS)
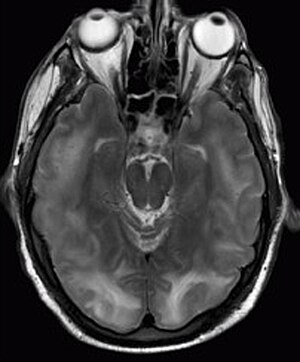
Síndrome de encefalopatia reversível posterior visível na ressonância magnética como corticos múltiplos -áreas subcorticais de sinal hiperintenso ponderado em T2 (branco) envolvendo os lobos occipital e parietal bilateralmente e ponte.
Neurologia
Convulsões, dor de cabeça, distúrbios visuais, estado mental alterado, às vezes fraqueza nos membros ou incapacidade de falar
Hemorragia intracraniana
A síndrome da encefalopatia reversível posterior (PRES), também conhecida como síndrome da leucoencefalopatia posterior reversível (RPLS), é uma condição rara na qual partes do cérebro são afetadas por edema, geralmente como resultado de uma causa subjacente. Alguém com PRES pode sentir dor de cabeça, alterações na visão e convulsões, com alguns desenvolvendo outros sintomas neurológicos, como confusão ou fraqueza de um ou mais membros. O nome da doença inclui a palavra “posterior” porque afeta predominantemente, embora não exclusivamente, a parte posterior do cérebro (os lobos parietal e occipital). As causas subjacentes comuns são pressão arterial gravemente elevada, insuficiência renal, infecções graves, certos medicamentos, algumas doenças autoimunes e pré-eclâmpsia. O diagnóstico geralmente é feito por varredura do cérebro (MRI) em que áreas de edema podem ser identificadas.
O tratamento para PRES é de suporte: remoção da causa ou causas e tratamento de qualquer uma das complicações, como anticonvulsivantes para convulsões. A PRES pode ser complicada por hemorragia intracraniana, mas é relativamente rara. A maioria das pessoas se recupera totalmente, embora algumas possam apresentar alguns sintomas residuais. A PRES foi descrita pela primeira vez em 1996.
Sinais e sintomas
A PRES geralmente tem um início agudo. A maioria das pessoas com PRES experimenta dores de cabeça e convulsões; muitos também apresentam alterações visuais, confusão e sonolência, fraqueza do braço e / ou perna em um lado do corpo (hemiplegia), dificuldade de falar ou, mais raramente, outros sintomas neurológicos. As alterações visuais na PRES podem incluir hemianopsia (incapacidade de ver a parte esquerda ou direita do campo visual), visão turva, falta de consciência visual de um lado, alucinações visuais e cegueira cortical.
Ocorrem convulsões em cerca de dois terços dos casos. Em crianças, isso é mais comum ainda, em 90%. Se ocorrerem convulsões, podem ser focais ou generalizadas. Uma pequena proporção desenvolve estado epiléptico, em que as crises não são controladas com medidas simples.
Causas
As causas que podem contribuir para o desenvolvimento de PRES são: imunossupressão (especialmente para transplante de órgãos, por exemplo com tacrolimus), infecção grave e / ou sepse, quimioterapia, doença autoimune e pré-eclâmpsia. A hipertensão está freqüentemente presente. Da mesma forma, a maioria das pessoas com PRES tem uma função renal prejudicada e 21% estão recebendo hemodiálise regular. Na PRES relacionada a medicamentos, pode haver um intervalo de semanas a meses entre o início do tratamento e o desenvolvimento da PRES. Após um transplante de células-tronco hematopoéticas (transplante de medula óssea), o risco de PRES é de aproximadamente 8%, enquanto o risco é menor (0,4-6%) após um transplante de órgão sólido.
As seguintes doenças autoimunes foram associada à PRES: púrpura trombocitopênica trombótica (TTP), colangite esclerosante primária (PSC), artrite reumatóide (AR), síndrome de Sjögren, poliarterite nodosa (PAN), esclerose sistêmica, lúpus eritematoso sistêmico (LES), granulomatose com polangiite ( GPA), doença de Crohn e neuromielite óptica (NMO), bem como síndrome hemolítico-urêmica (SHU). Uma série de outras associações também foram relatadas, incluindo alguns outros grupos de medicamentos, transfusão de sangue, níveis elevados de cálcio, diminuição níveis de magnésio, angiopatia cerebral pós-parto e drogas de abuso (cocaína e anfetamina).
Foi sugerido que a PRES é idêntica ou intimamente relacionada à encefalopatia hipertensiva, a presença de sintomas neurológicos naqueles com uma emergência hipertensiva.
Mecanismo
Embora o mecanismo preciso seja PRES não seja totalmente compreendido, considera-se que está relacionado a um problema com os vasos sanguíneos do cérebro. Existem várias teorias sobre o motivo pelo qual esses vasos sanguíneos podem se tornar inadequadamente permeáveis e permitir que o tecido cerebral circundante inche. A teoria “vasogênica” postula que a pressão sanguínea extremamente alta supera a capacidade normal dos vasos sanguíneos no cérebro de manter um fluxo sanguíneo cerebral normal. A pressão excessiva danifica a camada endotelial e a barreira hematoencefálica, levando ao inchaço (edema).Isso afeta predominantemente as partes “posteriores” do cérebro, que são mais suscetíveis. A teoria “vasogênica” parece explicar os quase 50% dos casos de PRES em que a pressão arterial estava gravemente elevada. É também chamada de teoria do “avanço” ou “teoria da hiperperfusão”. Essa teoria não explica o edema em muitos outros casos em que a pressão arterial está normal ou mesmo baixa; na verdade, o edema tende a ser mais grave naqueles sem pressão arterial anormalmente elevada.
Na PRES secundária a outras causas, o dano aos vasos sanguíneos foi atribuído a outros mecanismos. A teoria “citotóxica” sugere que é o dano celular direto por toxinas (geralmente medicamentos) que precipita o edema. A teoria “imunogênica” sugere um papel para o sistema imunológico (especificamente as células T). Alguns consideram as teorias citotóxica e imunogênica juntas como uma única teoria “tóxica”. Parece haver um papel das citocinas em causar disfunção endotelial.
Finalmente, de acordo com a teoria do “neuropeptídeo / vasoconstrição cerebral”, algumas substâncias específicas (endotelina 1, tromboxano A2) provocam espasmo dos vasos sanguíneos com danos resultantes da parede do vaso e edema. A última hipótese é apoiada pelo achado frequente de espasmos difusos dos vasos sanguíneos (vasoconstrição) em muitas pessoas com PRES e pela evidência de perfusão diminuída, embora o espasmo também possa ser uma consequência do dano ao vaso sanguíneo, e não a causa. Alguns, portanto, incluem o vasoespasmo na teoria “tóxica”. É considerado provável que todos esses mecanismos múltiplos potencialmente desempenham um papel no desenvolvimento de PRES.
Diagnóstico
Não há critérios diagnósticos formais para PRES, mas foi proposto que PRES pode ser diagnosticado se alguém desenvolveu sintomas neurológicos agudos (convulsão, estado mental alterado, dor de cabeça, distúrbios visuais) junto com um ou mais fatores de risco conhecidos, aparência típica em imagens cerebrais (ou imagens normais) e nenhum outro diagnóstico alternativo. Alguns consideram que as anormalidades precisam ser mostradas como reversíveis. Se a punção lombar for realizada, pode haver aumento dos níveis de proteína, mas não há leucócitos. A varredura de tomografia computadorizada pode ser realizada em primeiro lugar; isso pode mostrar áreas de substância branca de baixa densidade nos lobos posteriores.
O diagnóstico geralmente é feito por ressonância magnética do cérebro. Os achados mais característicos para PRES são hiperintensidades simétricas em imagens pesadas em T2 nos lobos parietal e occipital; esse padrão está presente em mais da metade de todos os casos. As sequências FLAIR podem mostrar melhor essas anormalidades. Alguns outros padrões raros específicos foram descritos: o padrão de bacia hidrográfica do sulco frontal superior (SFS), um padrão de bacia hidrográfica envolvendo todo o hemisfério (holo-hemisférico) e um padrão central com edema vasogênico na substância branca profunda, gânglios da base, tálamo, tronco cerebral e pons. Esses padrões distintos geralmente não se correlacionam com a natureza dos sintomas ou com sua gravidade, embora o edema grave possa sugerir um prognóstico pior. Se as aparências não forem típicas, outras causas para os sintomas e as anormalidades de imagem precisam ser consideradas antes que a PRES possa ser diagnosticada conclusivamente. Em muitos casos, há evidências de constrição dos vasos sanguíneos (se a angiografia for realizada), sugerindo uma possível sobreposição com a síndrome de vasoconstrição cerebral reversível (RCVS). A ressonância magnética por difusão pode ser usada para identificar áreas de edema citotóxico causado por fluxo sanguíneo insuficiente (isquemia), mas não está claro se isso é prognosticamente relevante. O coeficiente de difusão aparente anormal é observado em cerca de 20% dos casos.
Em 10–25% dos casos de PRES, há evidência de hemorragia na neuroimagem. Vários tipos de hemorragia podem ocorrer: hemorragia no próprio tecido cerebral (hemorragia intraparenquimatosa), hemorragia subaracnóide sulcal e microblangas.
Tratamento
Não há tratamento direto para PRES, exceto remover ou tratar qualquer causa subjacente. Por exemplo, pode ser necessário suspender a medicação imunossupressora. 40% de todas as pessoas com PRES não estão bem o suficiente para requerer internação na unidade de terapia intensiva para observação cuidadosa e tratamento de complicações. Aqueles com convulsões recebem anticonvulsivantes.
Se houver uma emergência hipertensiva, a pressão arterial é reduzida em 20-30% usando infusão contínua de um medicamento para baixar a pressão arterial com monitoramento rigoroso. Dos agentes redutores da pressão arterial disponíveis, os nitratos podem precisar ser evitados, pois existe a preocupação de que isso possa agravar a PRES, mesmo ao reduzir a pressão arterial. Na PRES secundária à pré-eclâmpsia, sulfato de magnésio pode ser administrado.
Prognóstico
Com tratamento adequado, 70-90% das pessoas com PRES recuperam-se totalmente em horas ou dias. 8–17% das pessoas com PRES morrem, embora nem sempre seja uma consequência direta do PRES.Daqueles que apresentam sintomas residuais após PRES, isso pode ser atribuído em grande parte à hemorragia. A não resolução das anomalias da ressonância magnética foi associada a resultados piores. Se a PRES foi causada por pré-eclâmpsia, o prognóstico é melhor do que na PRES devido a outras causas.
Os fatores que predizem um pior prognóstico são a idade da pessoa, o nível de proteína C reativa no sangue ( um marcador de inflamação), estado mental alterado no momento do diagnóstico e marcadores alterados de coagulação. Pessoas com diabetes podem ter um resultado pior, e anormalidades no corpo caloso na ressonância magnética foram associadas a pior prognóstico. Alguns padrões na eletroencefalografia ( EEG) também estão associados a um pior resultado.
Depois de um episódio de PRES, mesmo quando associado à atividade convulsiva, apenas uma pequena proporção de pessoas permanece em risco de convulsões contínuas e a maioria pode eventualmente interromper tratamento anticonvulsivante.
Epidemiologia
A incidência (número de casos por ano) de PRES não é conhecida, mas o uso crescente de exames de ressonância magnética levou a um maior reconhecimento.
História
O PRES foi descrito pela primeira vez em 1996 em um grupo de 15 pacientes identificados retrospectivamente nos prontuários do New England Medical Center em Boston e do Hôpital Sainte Anne em Paris. O nome foi revisado em 2000 de “leucencefalopatia” para “encefalopatia”, já que o primeiro sugeria que afetava apenas a substância branca do cérebro, o que não é o caso.
- CID-10: I67,83
- CID-9-CM: 348,39
- MeSH : D054038
- DiseasesDB: 10460
