Omkeerbaar posterieur leuko-encefalopathiesyndroom (RPLS)
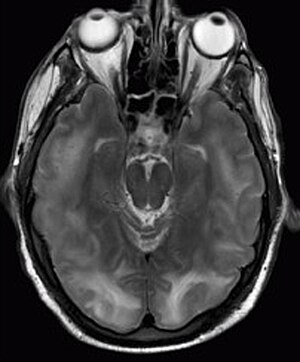
Posterieur reversibel encefalopathiesyndroom zichtbaar op MRI als multiple cortico -subcorticale gebieden van T2-gewogen hyperintens (wit) signaal waarbij de occipitale en pariëtale lobben bilateraal en pons betrokken zijn.
Neurologie
Aanvallen, hoofdpijn, visuele stoornissen, veranderde mentale toestand, soms zwakte van de ledematen of onvermogen om te spreken
Intracraniële bloeding
Posterieur reversibel encefalopathiesyndroom (PRES), ook bekend als reversibel posterieur leuko-encefalopathiesyndroom (RPLS), is een zeldzame aandoening waarbij delen van de hersenen worden aangetast door zwelling, meestal als gevolg van een onderliggende oorzaak. Iemand met PRES kan hoofdpijn, veranderingen in het gezichtsvermogen en epileptische aanvallen krijgen, waarbij sommige andere neurologische symptomen ontwikkelen, zoals verwardheid of zwakte van een of meer ledematen. De naam van de aandoening omvat het woord “posterieur” omdat het voornamelijk, maar niet uitsluitend, de achterkant van de hersenen (de pariëtale en occipitale lobben) beïnvloedt. Veel voorkomende onderliggende oorzaken zijn ernstig verhoogde bloeddruk, nierfalen, ernstige infecties, bepaalde medicijnen, sommige auto-immuunziekten en pre-eclampsie. De diagnose wordt meestal gesteld door middel van een hersenscan (MRI) waarop zwellinggebieden kunnen worden geïdentificeerd.
De behandeling van PRES is ondersteunend: verwijdering van de oorzaak of oorzaken en behandeling van een van de complicaties, zoals anticonvulsiva voor aanvallen. PRES kan worden gecompliceerd door intracraniële bloeding, maar dit is relatief zeldzaam. De meerderheid van de mensen herstelt volledig, hoewel sommigen enkele restsymptomen kunnen ervaren. PRES werd voor het eerst beschreven in 1996.
Tekenen en symptomen
PRES heeft meestal een acuut begin. De meeste mensen met PRES ervaren hoofdpijn en toevallen; velen ervaren ook visuele veranderingen, verwardheid en sufheid, zwakte van de arm en / of been aan één kant van het lichaam (hemiplegie), problemen met spreken, of zeldzamer andere neurologische symptomen. De visuele veranderingen bij PRES kunnen onder meer hemianopsie (onvermogen om het linker of rechter deel van het gezichtsveld te zien), wazig zien, gebrek aan visueel bewustzijn aan één kant, visuele hallucinaties en corticale blindheid omvatten.
Epileptische aanvallen komen voor. in ongeveer twee derde van de gevallen. Bij kinderen komt dit nog vaker voor, namelijk 90%. Als er aanvallen optreden, kunnen deze focaal of gegeneraliseerd zijn. Een klein deel ontwikkelt status epilepticus, waarbij aanvallen niet met eenvoudige maatregelen onder controle kunnen worden gehouden.
Oorzaken
Oorzaken die kunnen bijdragen aan de ontwikkeling van PRES zijn: immunosuppressie (vooral bij orgaantransplantatie, bijv. met tacrolimus), ernstige infectie en / of sepsis, chemotherapie, auto-immuunziekte en pre-eclampsie. Hoge bloeddruk is vaak aanwezig. Evenzo heeft de meerderheid van de mensen met PRES een verminderde nierfunctie en krijgt 21% regelmatig hemodialyse. Bij PRES gerelateerd aan medicatie kan er een interval van weken tot maanden zitten tussen het begin van de behandeling en de ontwikkeling van PRES. Na een hematopoëtische stamceltransplantatie (beenmergtransplantatie) is het risico op PRES ongeveer 8%, terwijl het risico lager is (0,4-6%) na een solide orgaantransplantatie.
De volgende auto-immuunziekten zijn gevonden geassocieerd te zijn met PRES: trombotische trombocytopenische purpura (TTP), primaire scleroserende cholangitis (PSC), reumatoïde artritis (RA), syndroom van Sjögren, polyarteritis nodosa (PAN), systemische sclerose, systemische lupus erythematosus (SLE), granulomatose met polyangiitis ( GPA), de ziekte van Crohn en neuromyelitis optica (NMO), evenals hemolytisch-uremisch syndroom (HUS). Er zijn ook een aantal andere associaties gemeld, waaronder enkele andere groepen medicijnen, bloedtransfusie, verhoogde calciumspiegels, verlaagde magnesiumspiegels, postpartum cerebrale angiopathie en drugsmisbruik (cocaïne en amfetamine).
Er is gesuggereerd dat PRES identiek is aan of nauw verband houdt met hypertensieve encefalopathie, de aanwezigheid van neurologische symptomen bij mensen met een hypertensieve noodsituatie.
Mechanisme
Hoewel het precieze mechanisme PRES niet volledig wordt begrepen, wordt aangenomen dat het verband houdt met een probleem met de bloedvaten van de hersenen. Er zijn verschillende theorieën over waarom deze bloedvaten ongepast doorlaatbaar kunnen worden en ervoor kunnen zorgen dat het omliggende hersenweefsel opgezwollen raakt. De “vasogene” theorie stelt dat extreem hoge bloeddruk het normale vermogen van bloedvaten in de hersenen overwint om een normale cerebrale bloedstroom te behouden. De overmatige druk beschadigt de endotheliale laag en de bloed-hersenbarrière, wat leidt tot zwelling (oedeem).Dit treft voornamelijk de “posterieure” delen van de hersenen die gevoeliger zijn. De “vasogene” theorie lijkt de bijna 50% van de gevallen van PRES te verklaren waarin sprake was van ernstig verhoogde bloeddruk. Het wordt ook wel de “doorbraak” -theorie of de “hyperperfusietheorie” genoemd. Deze theorie verklaart niet het oedeem in veel andere gevallen waarin de bloeddruk normaal of zelfs laag was; in feite is het oedeem meestal ernstiger bij mensen zonder abnormaal verhoogde bloeddruk.
In PRES, secundair aan andere oorzaken, wordt de bloedvatbeschadiging toegeschreven aan andere mechanismen. De “cytotoxische” theorie suggereert dat het oedeem wordt versneld door directe celbeschadiging door toxines (meestal medicijnen). De “immunogene” theorie suggereert een rol voor het immuunsysteem (specifiek T-cellen). Sommigen beschouwen de cytotoxische en immunogene theorieën samen als één enkele “giftige” theorie. Er lijkt een rol te zijn weggelegd voor cytokines bij het veroorzaken van endotheeldisfunctie.
Ten slotte, volgens de theorie van ‘neuropeptide / cerebrale vasoconstrictie’, veroorzaken sommige specifieke stoffen (endotheline 1, tromboxaan A2) spasmen van de bloedvaten met resulterende vaatwandschade en oedeem. De laatste hypothese wordt ondersteund door de frequente vondst van diffuse bloedvatkrampen (vasoconstrictie) bij veel mensen met PRES, en het bewijs voor verminderde perfusie, hoewel de spasmen ook een gevolg kunnen zijn van de bloedvatbeschadiging in plaats van de oorzaak. Sommige nemen daarom de vasospasme op in de “giftige” theorie. Het wordt waarschijnlijk geacht dat deze meerdere mechanismen mogelijk allemaal een rol spelen bij de ontwikkeling van PRES.
Diagnose
Er zijn geen formele diagnostische criteria voor PRES, maar er is voorgesteld dat PRES kan worden gediagnosticeerd als iemand acute neurologische symptomen heeft ontwikkeld (aanval, veranderde mentale toestand, hoofdpijn, visuele stoornissen) samen met een of meer bekende risicofactoren, typisch voorkomen op beeldvorming van de hersenen (of normale beeldvorming) en geen andere alternatieve diagnose. Sommigen zijn van mening dat moet worden aangetoond dat de afwijkingen omkeerbaar zijn. Als een lumbaalpunctie wordt uitgevoerd, kan dit wijzen op verhoogde eiwitniveaus, maar geen witte bloedcellen. Het scannen van computertomografie kan in eerste instantie worden uitgevoerd; dit kan witte stofgebieden met een lage dichtheid in de achterste kwabben vertonen.
De diagnose wordt doorgaans gesteld met behulp van magnetische resonantiebeeldvorming van de hersenen. De bevindingen die het meest kenmerkend zijn voor PRES zijn symmetrische hyperintensiteiten op T2-gewogen beeldvorming in de pariëtale en occipitale lobben; dit patroon is in meer dan de helft van alle gevallen aanwezig. FLAIR-sequenties kunnen deze afwijkingen beter laten zien. Enkele specifieke andere zeldzame patronen zijn beschreven: het stroomgebiedpatroon van de superieure frontale sulcus (SFS), een stroomgebiedpatroon dat het hele halfrond omvat (holohemisferisch) en een centraal patroon met vasogeen oedeem in de diepe witte stof, basale ganglia, thalami, hersenstam en pons. Deze verschillende patronen correleren doorgaans niet met de aard van de symptomen of hun ernst, hoewel ernstig oedeem een slechtere prognose kan suggereren. Als de uiterlijke kenmerken niet typisch zijn, moeten andere oorzaken van de symptomen en de beeldvormingsafwijkingen worden overwogen voordat PRES definitief kan worden vastgesteld. In veel gevallen zijn er aanwijzingen voor vernauwing van de bloedvaten (als angiografie wordt uitgevoerd), wat duidt op een mogelijke overlap met het reversibele cerebrale vasoconstrictie-syndroom (RCVS). Diffusie-MRI kan worden gebruikt om gebieden van cytotoxisch oedeem te identificeren die worden veroorzaakt door een slechte bloedstroom (ischemie), maar het is niet duidelijk of dit prognostisch relevant is. Abnormale schijnbare diffusiecoëfficiënt wordt gezien in ongeveer 20% van de gevallen.
In 10-25% van de gevallen van PRES is er bewijs van bloeding op neuroimaging. Er kunnen verschillende soorten bloeding optreden: bloeding in het hersenweefsel zelf (intraparenchymale bloeding), sulcale subarachnoïdale bloeding en microbloedingen.
Behandeling
Er is geen directe behandeling voor PRES, behalve het verwijderen of behandelen van een onderliggende oorzaak. Het kan bijvoorbeeld nodig zijn om immunosuppressieve medicatie te onthouden. 40% van alle mensen met PRES is zo ziek dat ze opname op de intensive care nodig hebben voor nauwkeurige observatie en behandeling van complicaties. Degenen met epileptische aanvallen krijgen anticonvulsiva toegediend.
Als er een hypertensieve noodsituatie is, wordt de bloeddruk met 20-30% verlaagd door middel van een continue infusie van een bloeddrukverlagend medicijn met nauwlettende controle. Van de beschikbare bloeddrukverlagende middelen kan het nodig zijn nitraten te vermijden, aangezien men zich zorgen maakt dat dit de PRES kan verergeren, zelfs bij verlaging van de bloeddruk. Bij PRES secundair aan pre-eclampsie kan magnesiumsulfaat worden toegediend.
Prognose
Met adequate behandeling herstelt 70-90% van de mensen met PRES binnen enkele uren tot dagen volledig. 8–17% van de mensen met PRES overlijdt, hoewel dit niet altijd een direct gevolg is van de PRES.Van degenen die restverschijnselen hebben na PRES, is dit grotendeels toe te schrijven aan bloeding. Het niet oplossen van MRI-afwijkingen is in verband gebracht met slechtere resultaten. Als PRES werd veroorzaakt door pre-eclampsie, is de prognose beter dan bij PRES vanwege andere oorzaken.
Factoren die een slechtere prognose voorspellen, zijn de leeftijd van de persoon, het niveau van C-reactief proteïne in het bloed ( een marker van ontsteking), veranderde mentale toestand op het moment van diagnose en veranderde markers van stolling. Mensen met diabetes kunnen een slechtere uitkomst hebben, en afwijkingen in het corpus callosum op MRI zijn in verband gebracht met een slechtere prognose. Sommige patronen op elektro-encefalografie ( EEG) worden ook in verband gebracht met een slechtere uitkomst.
Na een episode van PRES, zelfs wanneer dit werd geassocieerd met epileptische activiteit, blijft slechts een klein deel van de mensen het risico lopen op voortdurende aanvallen en de meerderheid kan uiteindelijk stoppen anticonvulsieve behandeling.
Epidemiologie
De incidentie (aantal gevallen per jaar) van PRES is niet bekend, maar toenemend gebruik van MRI-scans heeft geleid tot meer herkenning.
Geschiedenis
PRES werd voor het eerst beschreven in 1996 in een groep van 15 patiënten achteraf geïdentificeerd in de archieven van het New England Medical Center in Boston en Hôpital Sainte Anne in Parijs. De naam werd in 2000 herzien van “leukencephalopathy” naar “encephalopathy”, aangezien de eerste suggereerde dat het alleen de witte stof van de hersenen beïnvloedt, wat niet het geval is.
- ICD-10: I67.83
- ICD-9-CM: 348.39
- MeSH : D054038
- Ziekten DB: 10460
